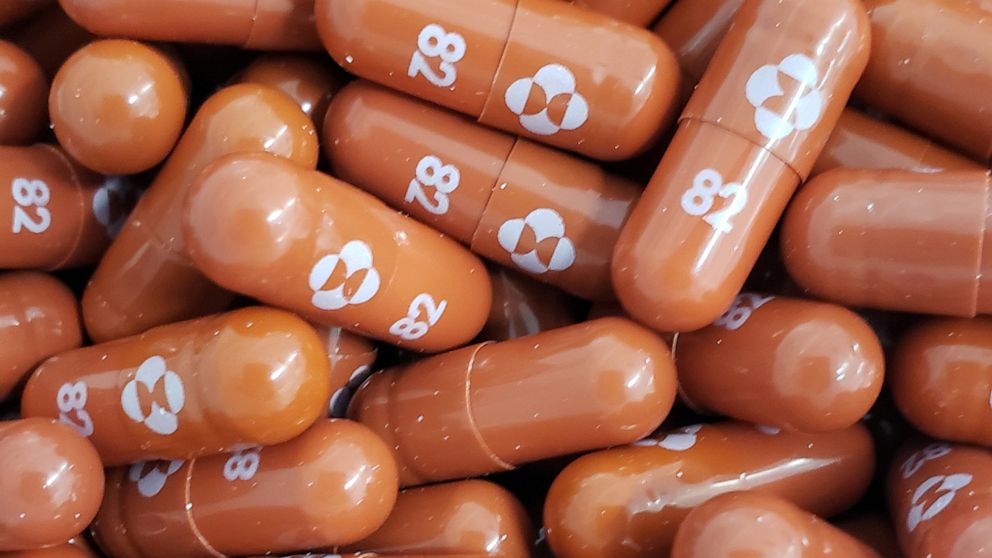
MERCK社のコロナ経口薬「モルヌピラビル」について知って置きたい事
2021年10月2日
モルヌピラビルは、インフルエンザの治療薬として開発されました。内部告発によると、モルヌピラビルには変異原性があり、DNAを変化させる可能性があるとされています。現在、モルヌピラビルはCOVID-19に再利用されている。メルク社はインドのメーカーと契約を結び、インド市場に参入する為に500万ドルの寄付を発表しました。ここでは、メルク社のコビット錠モルヌピラビルについて知って置くべき事をまとめました。
モルヌピラビルはインフルエンザの為に開発されました。
Molnupiravir(開発コード:MK-4482、EIDD-2801)は、経口投与可能な実験的抗ウイルス剤で、インフルエンザの治療薬として開発されました。
合成ヌクレオシド誘導体であるN4-ヒドロキシシチジンのプロドラッグであり、ウイルスのRNA複製時にコピーエラーを引き起こす事で抗ウイルス作用を発揮する。
本剤は、エモリー大学において、同大学のドラッグ・イノベーション・カンパニーである Drug Innovation Ventures at Emory(DRIVE)により開発されました。
その後、マイアミを拠点とする リッジバック・バイオセラピューティクス社 が買収し、後にメルク社と提携して更に開発を進めました。
モルヌピラビルはあなたのDNAを変えるかも知れません
2020年4月、本剤の承認前に生物医学先端研究開発機構(BARDA)の責任者を解任されたリック・ブライトは、同クラスの類似薬に変異原性があるとブライトが懸念していたにも関らず、リッジバックがBARDAに圧力をかけてEIDD-2801の製造資金を提供させたと主張する内部告発を提出しました。
モルヌピラビルの有効成分を調査していた以前の会社であるPharmasset社は、同様の懸念から調査を断念しています。
遺伝学では、生物の遺伝物質(通常はDNA)を恒久的に変化させ、その結果、突然変異の頻度を自然背景レベルよりも増加させる物理的または化学的な物質を変異原と呼んでいます。
多くの突然変異が癌を引き起こす可能性がある為、その様な突然変異誘発物質は発癌性物質となりますが、必ずしも全てがそうではありません。
全ての変異原は特徴的な突然変異のサインを持っており、一部の化学物質は細胞のプロセスを通じて変異原性を持つようになります。
3/5 one concern that it introduces virus mutations or potential mutagenic probably means it won’t be recommended in pregnancy. I seem to remember my good colleague @RickABright had a concern about this drug when he was at BARDA so maybe he can comment. Also important to remember
— Prof Peter Hotez MD PhD (@PeterHotez) October 1, 2021ウイルスの突然変異を誘発したり、変異原性があるのではないかという懸念があるため、妊娠中の使用は推奨されません。そういえば、私の良き同僚である RickABright がBARDAにいた頃、この薬について懸念していたのを覚えているので、彼がコメントしてくれるかもしれません。また、忘れてはならないのが
これに対し、DRIVE社のCEOである George Painter 氏は、モルヌピラビルの毒性試験が実施され、そのデータが米国および英国の規制当局に提供され、2020年春にヒトを対象とした安全性試験の実施が許可されたと述べ、この主張を否定しました。
その際、DRIVE社とRidgeback Biotherapeutics社は、今後、動物を用いた安全性試験を計画していることを明らかにしました。
メルク社のコビット経口薬 モルヌピラビル
2020年7月下旬、リッジバック・バイオセラピューティック社と開発で提携していたメルク社は、モルヌピラビルを2020年9月からの後期試験に移行させる意向を発表しました。
2020年10月19日、メルク社は、入院患者に焦点を当てた1年間のステージ2/3試験を開始しました。
2021年6月、米国保健社会福祉省は、米国食品医薬品局(FDA)から緊急使用許可(EUA)または承認を受けた場合、12億米ドル相当のモルヌピラビル(約170万コース)をメルク社から購入する事を約束しました。
2021年10月1日、メルク社は、COVID-19臨床試験を監視していた独立諮問委員会が、入院または死亡のリスクを48%減少させるという本剤の有用性を示す説得力のある証拠があるとして、試験への募集を早期に停止するよう勧告したと発表しました。
メルク社は、FDAにEUA(緊急使用許可)を求めると共に、世界の他の医薬品規制当局に販売申請を行う計画を発表しました。
また、メルク社は、本剤の供給を加速する為に、ジェネリック医薬品メーカーに本剤をライセンスする計画を発表しました。
メルク社のモルヌピラビルに関するインドとの契約について
メルク社は、インドの既存のジェネリック医薬品メーカー5社とモルヌピラビルの非独占的なボランタリー・ライセンス契約を締結したことを発表しました。
メルク社は、インド及びその他の低・中所得国(LMICs)において、現地規制当局による承認又は緊急承認を得た後、モルヌピラビルの供給を加速する為に、これらの契約を締結しました。
メルクの会長兼CEOであるケネス・C・フレイジャーは次のように述べています。
「今、インドで起きている」
「人間の苦しみの規模は壊滅的であり」
「それを軽減する為に」
「もっと多くの事をしなければならない事は明らかです」
「今回の合意は」
「モルヌピラビルの研究と並行して進めて来たもので」
「インドを始めとする」
「世界中でモルヌピラビルへのアクセスを促進するのに役立ちます」
「メルクは、インドの人々に救済をもたらし」
「最終的にパンデミックを終息させる為に」
「世界的な対応を支援する事を約束します」
これらのジェネリック医薬品メーカーは、世界保健機関(WHO)の事前認証を受けた製造施設を持ち、世界各国や中南米の主要な調達先への主要な供給者としての経験を有しています。
本契約に基づき、メルク社はこれらのメーカーにライセンスを供与し、インド及び100以上のLMICsにモルヌピラビルを供給します。
また、メルクは、追加ライセンスの可能性を探るため、Medicines Patent Poolと協議しています。
また、メルク社は、インドでの救援活動を支援する為に、500万ドル相当の酸素発生装置、マスク、手指消毒剤、資金援助などを寄付する予定です。
日本での報道のされ方