The People's Voice:mRNA Jab ‘Off Switch’ Discovered by Scientists – Media Blackout June 17, 2024 Sean Adl-Tabatabaiより転載します。
貼り付け開始、翻訳はDeeplさんです。
*** Translated with www.DeepL.com/Translator (free version) ***
https://thepeoplesvoice.tv/mrna-jab-off-switch-discovered-by-scientists-media-blackout/
mRNAジャブ(新型コロナ遺伝子ワクチン)の「オフスイッチ」が科学者によって発見される - Media Blackout
2024年6月17日 ショーン・アドル・タバタバイ
新しいプレプリント研究は、コビッドmRNA注射(新型コロナ遺伝子ワクチン、以下同)の遺伝子改変効果を不活性化する方法を詳述しており、この実験的注射によってダメージを受けた数十億の人々に希望の光を与えている。
『ファイザーバイオンテックとモデルナの生体内分布研究は、ナノ脂質結合したnms-mRNAが三角筋や腋窩リンパ節に残存するという主張を否定している。様々な組織で検出可能なワクチンmRNAレベルが残存していることは、潜在的な安全性の懸念を引き起こします。「ワクチンmRNAが宿主ゲノムに組み込まれる可能性と、リードスルーによる意図しないタンパク質産生が予想されることから、残存する合成mRNAを除去し、有害なスパイクタンパク質産生を停止させるメカニズムが提唱されている。ワクチンmRNAを標的にして分解するsiRNAとRIBOTACの使用は、健康への悪影響を軽減する有望なアプローチである。siRNAやRIBOTACを目的のmRNAを標的とするように容易に調整できることから、これらの技術は特に魅力的であるが、オフターゲット効果や免疫系活性化の可能性などの課題に対処するためにさらなる調査が必要である。』
Infowars.comが伝えている:メッセンジャーRNA(mRNA)技術は、Modernaの特許では修飾mRNAあるいは修飾メッセンジャーRNAを意味するmmRNAと呼ばれており、変更されたRNA配列を脂質ナノ粒子内にカプセル化し、被接種者の細胞に導入するエキゾチックな技術である。外来の人工的な配列がワクチン接種を受けた人の細胞に組み込まれるため、従来のワクチンというよりは遺伝子治療として機能する。
その個体がスパイクタンパク質を生成するのを永遠に止める方法はない。少なくともこれまでは。
この研究では、スパイクタンパク質の産生を止める方法について述べている。
「...カプセル化されたmRNAの寿命は長く、有害で致死的なスパイク(S)タンパク質を無制限に産生するため、潜在的な悪影響を軽減する戦略が必要である。「ここでは、残存する持続性ワクチンmRNAを標的とし、不活性化し、分解する有望な解決法として、small interfering RNA(siRNA)とリボヌクレアーゼ標的化キメラ(RIBOTAC)の可能性を探ります。siRNAとRIBOTACの標的化された性質は、正確な介入を可能にし、mRNAに基づく治療の有害事象を予防・軽減する道を提供する。"
この研究では、「siRNAとRIBOTACの応用」の項で、研究者たちが提案したコビドワクチンの変異原性効果をオフにする方法について詳しく述べている。


研究者たちはまた、提案された新しい治療法を図解で説明した。
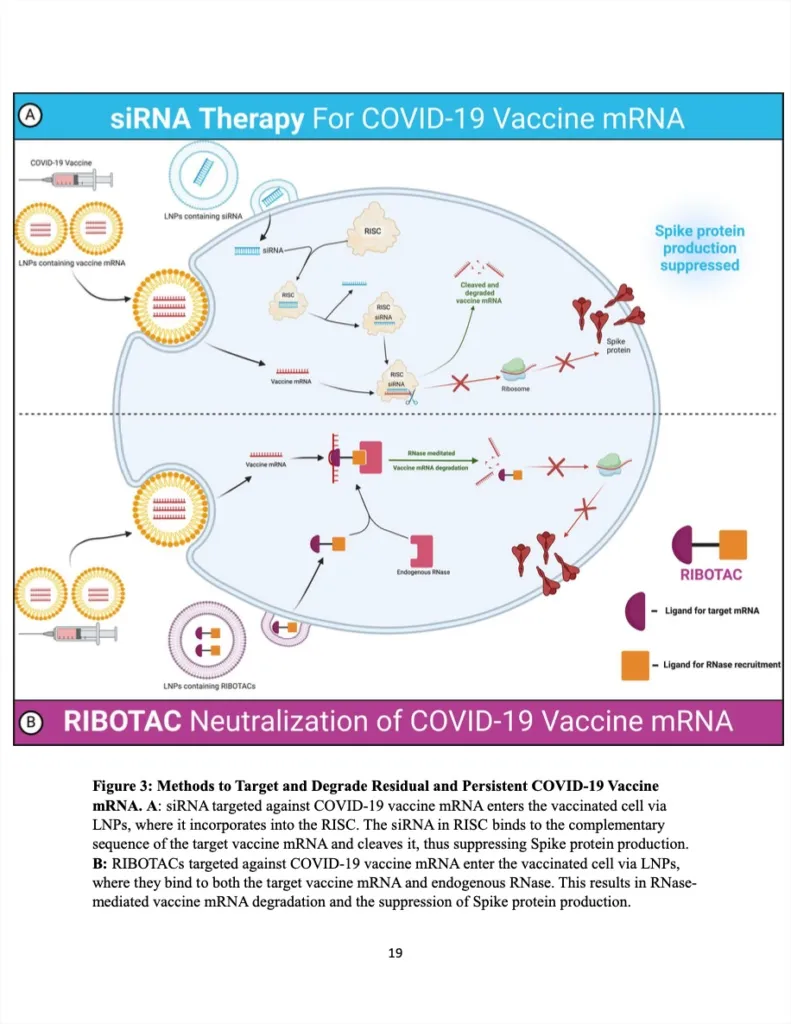
外来のメッセンジャーRNAは体内で容易に分解されるため、モデルルナ社(ファイザー社が模倣して訴えられたmRNAコビッドワクチンを開発した)は、mRNAペイロードを脂質ナノ粒子内にカプセル化し、細胞のリボソームへの輸送を可能にする方法を考案した。この研究では、エキゾチックなmRNAワクチン技術がヒトゲノムを改変するために、いかに多くの異なる身体システムを克服しなければならなかったかが述べられている。
「2020年にModerna(mRNA-1273)とPfizer-BioNTech(BNT162b2)のmRNAワクチンが承認される前に、mRNA技術に内在する限界を回避するために多くの課題が解決されました。研究者は以前、核酸をカプセル化し、ポリマー粒子を介して送達することに成功したことを実証したが、効果的な治療薬としてのmRNAの出現には、mRNAの不安定性と免疫原性を緩和し、さらにmRNAが複数の障壁を通過する能力が必要であった[1, 2]。mRNAが細胞外空間や標的細胞のヌクレアーゼを回避しても、mRNAのほとんどはエンドソームに捕捉され、その後分解される[3]。さらに、外来mRNAのエンドサイトーシスは、mRNAの翻訳を阻害し、mRNAの安定性を低下させることにより、パターン認識受容体を介した免疫原性を誘導する可能性がある[4-8]。さらに、mRNAの効率的な送達は、mRNAと細胞膜の負電荷によって妨げられる[2]。投与されたmRNAは、マクロファージの貪食作用や腎濾過によって除去されることもあります[2]」と、この研究は「はじめに」のセクションで述べている。
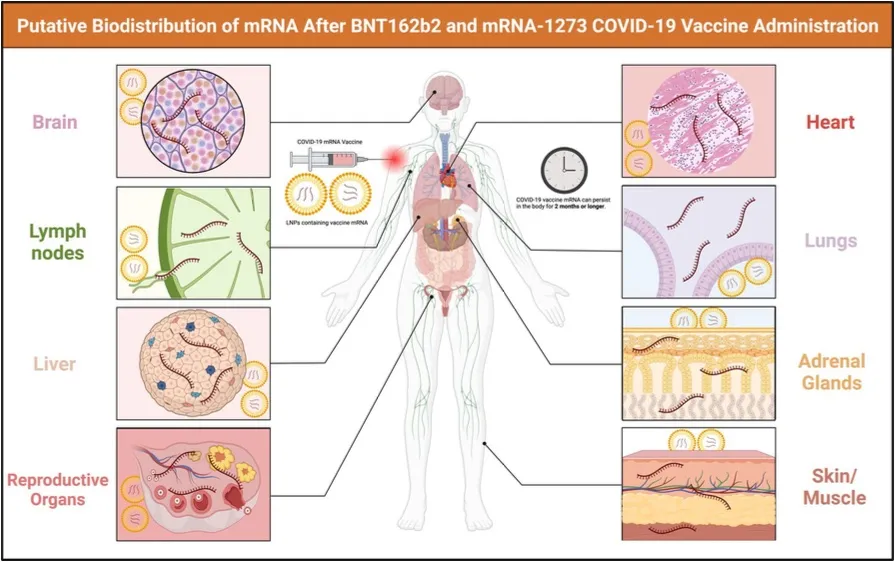
研究では、被接種者の体内におけるmRNAの分布の広がりについて論じている。「マウスモデルを用いたPardiらの研究では、皮下、筋肉内、皮内に注射されたLNPカプセル化mRNAが最大10日間移行することが示されている。驚くべきことに、mRNA-1273またはBNT162b2 mRNAワクチン投与後28日までの患者の血液中に、ワクチンSARS-CoV-2 Spike mRNAの全長または断片が9.3%観察された[45]。著者らは、血漿中に検出されたmRNAはLNPに包まれていると推測している。同様に、mRNA-1273またはBNT162b2の2回目の投与から60日後に、リンパ節の胚中心でワクチンmRNAが観察された[46]。さらに、Hannaらの研究は、ワクチンmRNAが注射部位から全身に分布するという以前の知見を立証している。BNT162b2またはmRNA-1273 COVID-19ワクチンを接種した13人の授乳婦の母乳を、ワクチンmRNAについて評価した。ワクチン接種後45時間までの母乳サンプルからは、完全性が低下した微量のワクチンmRNAが検出されました[47]」と、この研究は「Detection of Vaccine mRNA In Vivo」の項で述べている。
https://rumble.com/embed/v4zndfo/?pub=4

貼り付け終わり、
*** Translated with www.DeepL.com/Translator (free version) ***
https://thepeoplesvoice.tv/mrna-jab-off-switch-discovered-by-scientists-media-blackout/
mRNAジャブ(新型コロナ遺伝子ワクチン)の「オフスイッチ」が科学者によって発見される - Media Blackout
2024年6月17日 ショーン・アドル・タバタバイ

新しいプレプリント研究は、コビッドmRNA注射(新型コロナ遺伝子ワクチン、以下同)の遺伝子改変効果を不活性化する方法を詳述しており、この実験的注射によってダメージを受けた数十億の人々に希望の光を与えている。
『ファイザーバイオンテックとモデルナの生体内分布研究は、ナノ脂質結合したnms-mRNAが三角筋や腋窩リンパ節に残存するという主張を否定している。様々な組織で検出可能なワクチンmRNAレベルが残存していることは、潜在的な安全性の懸念を引き起こします。「ワクチンmRNAが宿主ゲノムに組み込まれる可能性と、リードスルーによる意図しないタンパク質産生が予想されることから、残存する合成mRNAを除去し、有害なスパイクタンパク質産生を停止させるメカニズムが提唱されている。ワクチンmRNAを標的にして分解するsiRNAとRIBOTACの使用は、健康への悪影響を軽減する有望なアプローチである。siRNAやRIBOTACを目的のmRNAを標的とするように容易に調整できることから、これらの技術は特に魅力的であるが、オフターゲット効果や免疫系活性化の可能性などの課題に対処するためにさらなる調査が必要である。』
Infowars.comが伝えている:メッセンジャーRNA(mRNA)技術は、Modernaの特許では修飾mRNAあるいは修飾メッセンジャーRNAを意味するmmRNAと呼ばれており、変更されたRNA配列を脂質ナノ粒子内にカプセル化し、被接種者の細胞に導入するエキゾチックな技術である。外来の人工的な配列がワクチン接種を受けた人の細胞に組み込まれるため、従来のワクチンというよりは遺伝子治療として機能する。
その個体がスパイクタンパク質を生成するのを永遠に止める方法はない。少なくともこれまでは。
この研究では、スパイクタンパク質の産生を止める方法について述べている。
「...カプセル化されたmRNAの寿命は長く、有害で致死的なスパイク(S)タンパク質を無制限に産生するため、潜在的な悪影響を軽減する戦略が必要である。「ここでは、残存する持続性ワクチンmRNAを標的とし、不活性化し、分解する有望な解決法として、small interfering RNA(siRNA)とリボヌクレアーゼ標的化キメラ(RIBOTAC)の可能性を探ります。siRNAとRIBOTACの標的化された性質は、正確な介入を可能にし、mRNAに基づく治療の有害事象を予防・軽減する道を提供する。"
この研究では、「siRNAとRIBOTACの応用」の項で、研究者たちが提案したコビドワクチンの変異原性効果をオフにする方法について詳しく述べている。


研究者たちはまた、提案された新しい治療法を図解で説明した。

外来のメッセンジャーRNAは体内で容易に分解されるため、モデルルナ社(ファイザー社が模倣して訴えられたmRNAコビッドワクチンを開発した)は、mRNAペイロードを脂質ナノ粒子内にカプセル化し、細胞のリボソームへの輸送を可能にする方法を考案した。この研究では、エキゾチックなmRNAワクチン技術がヒトゲノムを改変するために、いかに多くの異なる身体システムを克服しなければならなかったかが述べられている。
「2020年にModerna(mRNA-1273)とPfizer-BioNTech(BNT162b2)のmRNAワクチンが承認される前に、mRNA技術に内在する限界を回避するために多くの課題が解決されました。研究者は以前、核酸をカプセル化し、ポリマー粒子を介して送達することに成功したことを実証したが、効果的な治療薬としてのmRNAの出現には、mRNAの不安定性と免疫原性を緩和し、さらにmRNAが複数の障壁を通過する能力が必要であった[1, 2]。mRNAが細胞外空間や標的細胞のヌクレアーゼを回避しても、mRNAのほとんどはエンドソームに捕捉され、その後分解される[3]。さらに、外来mRNAのエンドサイトーシスは、mRNAの翻訳を阻害し、mRNAの安定性を低下させることにより、パターン認識受容体を介した免疫原性を誘導する可能性がある[4-8]。さらに、mRNAの効率的な送達は、mRNAと細胞膜の負電荷によって妨げられる[2]。投与されたmRNAは、マクロファージの貪食作用や腎濾過によって除去されることもあります[2]」と、この研究は「はじめに」のセクションで述べている。
研究では、被接種者の体内におけるmRNAの分布の広がりについて論じている。「マウスモデルを用いたPardiらの研究では、皮下、筋肉内、皮内に注射されたLNPカプセル化mRNAが最大10日間移行することが示されている。驚くべきことに、mRNA-1273またはBNT162b2 mRNAワクチン投与後28日までの患者の血液中に、ワクチンSARS-CoV-2 Spike mRNAの全長または断片が9.3%観察された[45]。著者らは、血漿中に検出されたmRNAはLNPに包まれていると推測している。同様に、mRNA-1273またはBNT162b2の2回目の投与から60日後に、リンパ節の胚中心でワクチンmRNAが観察された[46]。さらに、Hannaらの研究は、ワクチンmRNAが注射部位から全身に分布するという以前の知見を立証している。BNT162b2またはmRNA-1273 COVID-19ワクチンを接種した13人の授乳婦の母乳を、ワクチンmRNAについて評価した。ワクチン接種後45時間までの母乳サンプルからは、完全性が低下した微量のワクチンmRNAが検出されました[47]」と、この研究は「Detection of Vaccine mRNA In Vivo」の項で述べている。

https://rumble.com/embed/v4zndfo/?pub=4

貼り付け終わり、