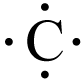下記はCK12という教育サイトからの引用です。中1〜高1レベルの化学です。日本国内トップレベルの高校生、いや中学生ならさらっと意味がわかるはずです。万一、分からないようなら学校で習っている英語は全くの無駄ということです。そんな授業を受け続けていても何の役にも立ちません。何のために英語を勉強するか?というPhilosophyが欠如しているからです。今の時代、生成AIがどんどん進歩しています。GeminiやChat GPTを使えばちゃんとした英語が勉強できます。そんな時代になったと言うのに学校や塾、予備校でダラダラと授業を受け続けているようでは来るべき2027年〜2030年頃に起こるであろう社会変化の潮流に乗れないでしょう。いや、乗れないでしょう、ではなく確実に乗れません。
Valence Electrons
Valence electrons are the electrons in the outer energy level of an atom and can participate in interactions with other atoms. Valence electrons are generally the electrons that are farthest from the nucleus. As a result, they may be attracted as much or more by the nucleus of another atom than they are by their own nucleus.
Electron Dot Diagrams of Elements
Because valence electrons are so important, atoms are often represented by simple diagrams that show only their valence electrons. These are called electron dot diagrams and three such diagrams are shown below. In this type of diagram, an element's chemical symbol is surrounded by dots that represent the valence electrons. Typically, the dots are drawn as if there is a square surrounding the element symbol with up to two dots per side. An element never has more than eight valence electrons, so there can’t be more than eight dots per atom.
Q: Carbon has four valence electrons. What does an electron dot diagram for this element look like?
A: An electron dot diagram for carbon looks like this:
How to Find Valence Electrons of Elements?
The number of valence electrons of an atom is reflected by its position in the periodic table of the elements (see Figure below). Across each row or period of the periodic table, the number of valence electrons in groups 1–2 and 13–18 increases by one from each element to the next. Within each column or group of the table, all the elements have the same number of valence electrons. This explains why all the elements in the same group have very similar chemical properties.