https://nordot.app/786077797867945984?c=39546741839462401
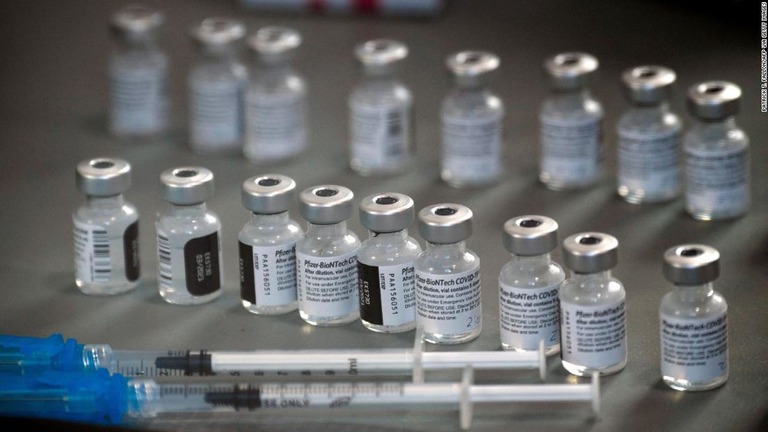
ワクチン追加接種、現時点で不要
米CDCとFDAが共同声明
共同通信社
【ワシントン共同】米疾病対策センター(CDC)と食品医薬品局(FDA)は8日、新型コロナウイルスのワクチンを規定の回数接種した人は、現時点で追加接種する必要はないとする共同声明を発表した。
インドで見つかり感染力が強いとされるデルタ株が米国でも急速に広がっているが、声明は「接種を完了していればデルタ株などの変異株に対しても重症化や死亡から守られる」とした。
声明は「新型コロナ入院患者や死者は事実上、全てワクチン未接種の人だ」とし、速やかにワクチンを接種するよう促した。今後追加接種が必要になるかどうかはCDCなどが科学的にデータを評価して決めるとしている。
************************************************************
https://www.bloomberg.co.jp/news/articles/2021-07-08/QVY2CWT0G1KY01?srnd=cojp-v2
************************************************************
https://news.yahoo.co.jp/pickup/6398222
ドルステン氏は、イスラエルと英国のデータに基づくと、抗体レベルが下がってもなお、重症化を防ぐワクチンの効果は引き続き
95%前後あると強調。
さらにファイザーの独自調査で、3回の接種を受ければ抗体レベルが2回接種時の5─10倍に跳ね上がり、期待される効果を発揮することがうかがえると付け加えた。
************************************************************
https://www.cnn.co.jp/business/35173631.html?ref=rss
************************************************************
東京都公式ホームページ
https://www.metro.tokyo.lg.jp/tosei/hodohappyo/press/2021/01/07/07.html
![]()
2021年01月07日 (公財)東京都医学総合研究所, 福祉保健局, 滋賀医科大学
ワクシニアウイルスベクターを用いた新型コロナウイルスワクチンの開発
動物実験による効果を確認しました
国産ワクチンを待つ人へ「打てる時期」「安全性」「効果」を徹底調査
【NEWSポストセブンプレミアム記事】
ファイザーに続き、モデルナやアストラゼネカが承認され、外国産コロナワクチン接種が加速している。しかし、安全性への不安から二の足を踏む“慎重派”も多い。そんな中、待望論が高まるのが国産ワクチンだ。
国産ワクチンは、5月時点で5社(米ノババックスから技術移転を受けて国内生産を目指している武田薬品工業を含む)が臨床試験を実施している。
その中で、ファイザーやモデルナと同じ「mRNA(メッセンジャーRNA)ワクチン」を開発しているのが第一三共だ。長崎大学大学院教授で日本ワクチン学会理事の森内浩幸氏が指摘する。
「ウイルスの遺伝情報物質であるmRNAを体に打ち込み、免疫反応を呼び起こすワクチンです。ファイザーやモデルナと第一三共の違いは、mRNAを包む膜にある。独自技術を用いた材料を使用しているので、接種後の炎症が生じにくくなることが期待されます。
もともとmRNAワクチンは新型コロナで初めて実用化されたものですが、第一三共のワクチンはそれに改善を加えた『第二世代』となります」
接種で感染リスクがどれほど減ったかを示す「有効率」は、ファイザー製が94.6%、モデルナ製が94.1%と好成績が報告されており、第一三共には両社以上に高い有効性が期待されている。
昨年6月、国内でいち早く臨床試験に着手したアンジェスは「DNAワクチン」の開発を目指している。
「人工的に合成したコロナウイルスのDNAそのものを体に打ち込み、免疫反応を呼び起こすワクチンです。現在、臨床試験は3段階のうち2段階目にあたる第2/第3相試験に入っており、国内で最も先行している。ただし、DNAワクチンはまだ世界で承認・実用化された例がありません」(森内氏)
第一三共やアンジェスのような遺伝子を打ち込むタイプのワクチンは製造面での利点が大きい。
「遺伝子情報を利用するため、実物の新型コロナウイルスを使用しなくても製造できます。そのため従来のワクチンに比べて、短期間で大量生産できる」(関西福祉大学教授の勝田吉彰氏)
安全性か、スピードか
KMバイオロジクスは「不活化ワクチン」の開発に挑んでいる。
mRNAワクチンやDNAワクチンなど遺伝子を使用するタイプとは異なり、不活化ワクチンは、感染性や病原性を消失させたウイルスそのものを体内に注入し、免疫反応を誘導する。
「最も古いタイプのワクチンのひとつで、KMバイオロジクスには同様の手法で日本脳炎のワクチンなどを製造した実績があります。歴史が古く、同タイプのワクチンが多く作られているため安全性の面で信頼度が高いと言えます。
欠点は、ウイルスそのものを培養するので製造に時間がかかること。これまでの不活化ワクチンの例を考えると、mRNAタイプより有効率が落ちる可能性があります」(森内氏)
KMバイオロジクスの広報担当者は安全性に自信を見せる。
「一般的に不活化ワクチンの副反応のほとんどは接種した部分の腫れや痛み程度で、全身性の症状が出ることはまれ。現時点では重篤な副反応は確認されていません。予測される副反応は限定的だと考えています」
5月10日の決算説明会で「年内にも供給を始めたい」と宣言した塩野義製薬と武田薬品工業(ノババックス)が開発を進めるのは「組み換えたんぱく質ワクチン」だ。
「遺伝子組み換え技術を使って合成したコロナウイルスのたんぱく質を打ち込むことで、免疫反応を呼び起こします。B型肝炎ウイルスワクチンで用いられる手法で、実績があり安全面も期待できますが、不活化ワクチンと同様にmRNAタイプのワクチンより有効性は落ちる可能性があります」(森内氏)
しかし、不活化ワクチンと組み換えたんぱく質ワクチンはmRNAワクチンがマイナス90度やマイナス20度で管理する必要があるのに対し、2~8度で保管できる設計のため、医療機関の設備投資のハードルが低いという利点がある。
なお国内では、アストラゼネカと同じ「ウイルスベクターワクチン」は開発のメドが立っていない。臨床試験受託大手のアイロムグループが、今年5月までに治験を目指していたが、10月以降に先送りになった。
「無害なウイルスにコロナウイルスの遺伝子情報を組み込んで投与するタイプで、過去にエボラウイルスのワクチンとして実用化された。国内で開発が進まないのは技術力や規制など、何らかの障壁があるからと考えられます」(勝田氏)
毎年打つことになる?
国産ワクチンの開発が、世界に比べ大きく遅れをとったことは否めない。それでも実用化を急ぐことは重要だ。
「新型コロナの流行は今年収束するとは限らない。これからインフルエンザワクチンのように毎年接種が必要になる可能性もある。この先、さらなる変異型ウイルスが出て感染爆発が起きれば、再びワクチン不足になることも考えられます。
さらに今後、新たな感染症が発生することも考慮すれば、国内で開発・生産体制を整えておくことは必要不可欠です。
これまでは薬事承認のハードルが高く国産ワクチンの開発が遅れましたが、現在、政府は他国との大規模治験の仕組みづくりや薬事承認手続きの簡略化を進めている。今後、予想よりも早く国産ワクチンが承認される可能性は十分あります」(勝田氏)
一刻も早い実用化を期待したい。
※週刊ポスト2021年6月11日号