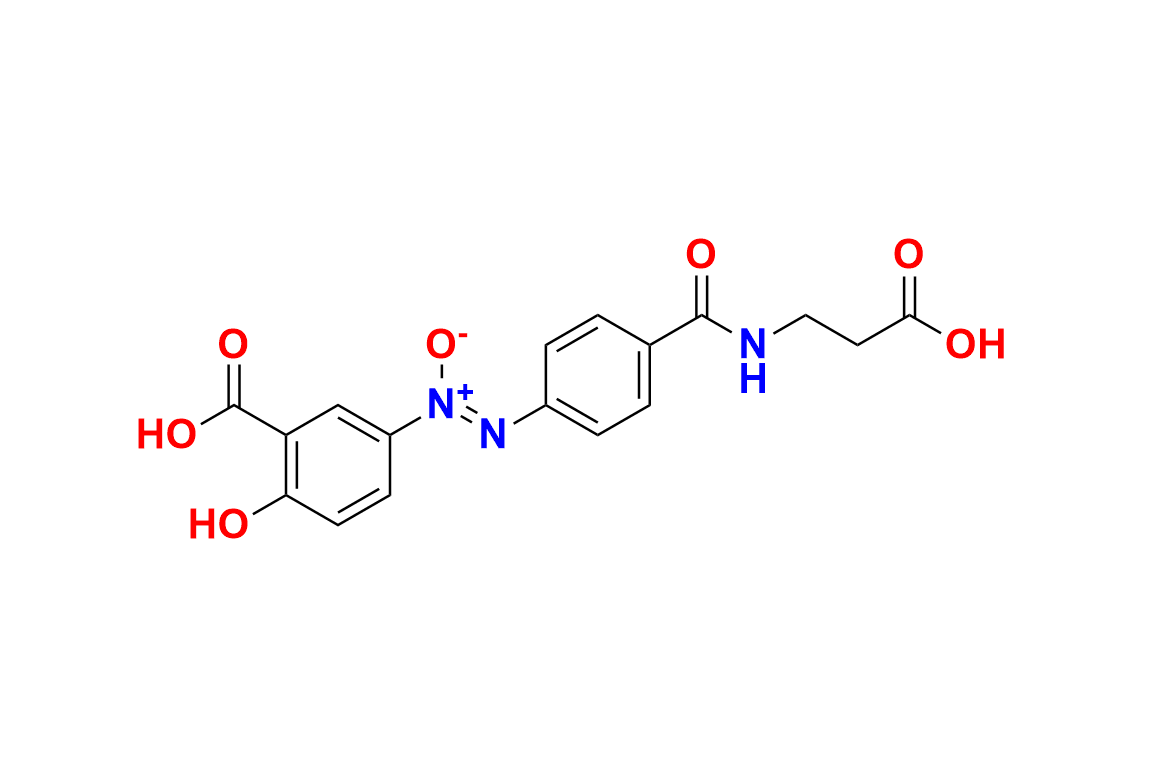
医薬品開発の分野において、有効成分(API)中の不純物を理解し管理することは、安全性と有効性を確保するうえで極めて重要です。Balsalazide Disodium(バルサラジドナトリウム)の合成および品質管理において注目すべき不純物の一つが、Balsalazide USP Impurity 1(バルサラジド USP 不純物1)です。
本記事では、この不純物の概要、形成要因、分析方法、そして規制上の重要性について詳しく解説します。
Balsalazide USP Impurity 1とは?
Balsalazide USP Impurity 1は、米国薬局方(USP)において公式に記載されている、Balsalazide Disodiumの合成や分解過程で発生する構造類似の副生成物です。微量であっても、医薬品の最終製品に含まれることで安全性や効果に影響を与える可能性があるため、その特定と管理が重要となります。
生成の背景と要因
Balsalazide Disodiumはメサラジン(5-ASA)のプロドラッグで、主に潰瘍性大腸炎などの炎症性腸疾患の治療に用いられます。腸内のアゾ還元酵素により分解され、有効成分を放出します。
このAPIの合成中に、副反応や未完了の結合反応などにより、Balsalazide USP Impurity 1のような不純物が生成されることがあります。具体的には以下の要因が挙げられます:
-
結合反応の不完全性
-
酸化分解
-
不純な出発原料
-
保管条件や経時変化による分解
構造が類似しているため、これらの不純物の分離と特定には高度な分析技術が求められます。
分析技術と検出方法
Balsalazide USP Impurity 1の特定と定量には、以下のような高度な分析技術が用いられます:
-
高速液体クロマトグラフィー(HPLC)
-
USPモノグラフに準拠した標準分析法
-
-
LC-MS(液体クロマトグラフィー質量分析)
-
分子量の確認と未知不純物の同定に有効
-
-
NMR(核磁気共鳴)分光法
-
詳細な構造情報を提供
-
-
IR(赤外線)分光法
-
官能基の同定に使用
-
これらの分析方法は、FDA、EMA、ICHなどの規制機関によって定められた厳格な基準に基づいて実施されます。
規制上のガイドラインと基準値
Balsalazide USP Impurity 1のような不純物には、以下の国際的なガイドラインが適用されます:
-
ICH Q3A(R2) – 新規原薬中の不純物
-
ICH Q3B(R2) – 新規製剤中の不純物
-
USPガイドライン – 不純物の限度値および識別基準を定める
通常、不純物がAPIの総重量の**0.10%**を超える場合には、その特定と毒性評価が義務づけられます。Balsalazide DisodiumのUSPモノグラフでは、不純物1を含む特定不純物の限度値が記載されています。
毒性と安全性への影響
Balsalazide USP Impurity 1は微量で存在することが多いですが、その薬理学的・毒性学的影響は慎重に評価される必要があります。懸念される点は以下のとおりです:
-
遺伝毒性
-
アレルギー性反応
-
代謝への悪影響
このため、医薬品のライフサイクル全体において不純物プロファイルの確立が不可欠です。
Balsalazide N-Oxide:もう一つの重要な不純物
Balsalazide N-Oxide(バルサラジドN-オキシド)は、Balsalazide Disodiumの酸化によって形成される、別の代表的な不純物です。こちらも構造的に類似しており、薬局方に基づいて厳格に監視される対象となっています。
Balsalazide USP Impurity 1と並んで、Balsalazide N-Oxideの理解と管理も製薬業界において重要です。
医薬品開発と品質管理における意義
Balsalazide USP Impurity 1の管理は以下の目的で不可欠です:
-
製品の安全性と有効性の確保
-
規制遵守の達成
-
製造ロット間の一貫性
-
安定性試験への対応
国際的な規制が進化する中で、製薬製造の透明性と品質保証の強化が求められており、不純物の管理はその要となっています。
まとめ
Balsalazide USP Impurity 1は量的にはごくわずかであっても、医薬品の品質と安全性において大きな意味を持つ存在です。精密な分析技術と厳格な規制基準のもとで、製薬メーカーはこのような不純物をしっかりと管理し、患者に安全な医薬品を提供しています。
この不純物の背後にある主成分について詳しく知りたい方は、**
**に関する完全ガイドもぜひご覧ください。