ESMO(ヨーロッパ臨床腫瘍学会)で発表されたKEYNOTE-A18試験の結果を受けてFDA(アメリカ食品医薬品局)が2024年1月12日に、CCRT(放射線同時化学療法)に併用するペンブロリズマブを承認したようです。いよいよ子宮頸がんの初回治療に免疫チェックポイント阻害薬(ICI)が入ってきました。
KENOTE-A18 試験:局所進行子宮頸癌に対しCCRTにペムブロリズマブを併用することで無増悪生存期間(PFS)を延長した試験
- 未治療の子宮頸がん患者でFIGO2014 stage IB2~IIB期のリンパ節転移陽性、FIGO2014 stage III~IVAが対象となりました。
- 多施設共同無作為化二重盲検プラセボ対照試験です。
- CCRT+ペンブロリズマブ群(529人)とCCRT+プラセボ群(531人)に無作為に1:1に割り付られました。
- ペンブロリズマブは、200mgを3週間ごとに5サイクル投与し、その後400mgを6週間ごとに15サイクル投与しました
- CCRTはシスプラチン40mg/m2を週1回点滴静注で5-6サイクル、外部照射療法後に小線源療法を行いました。
- 主要評価項目は無増悪生存期間(PFS)および全生存期間(OS)でした。
- 全集団においてPFSが統計学的に有意に改善したことが示されました。
- OSは有意な差にはならなかったものの、ペムブロリズマブ併用群で良好な傾向が示されました。
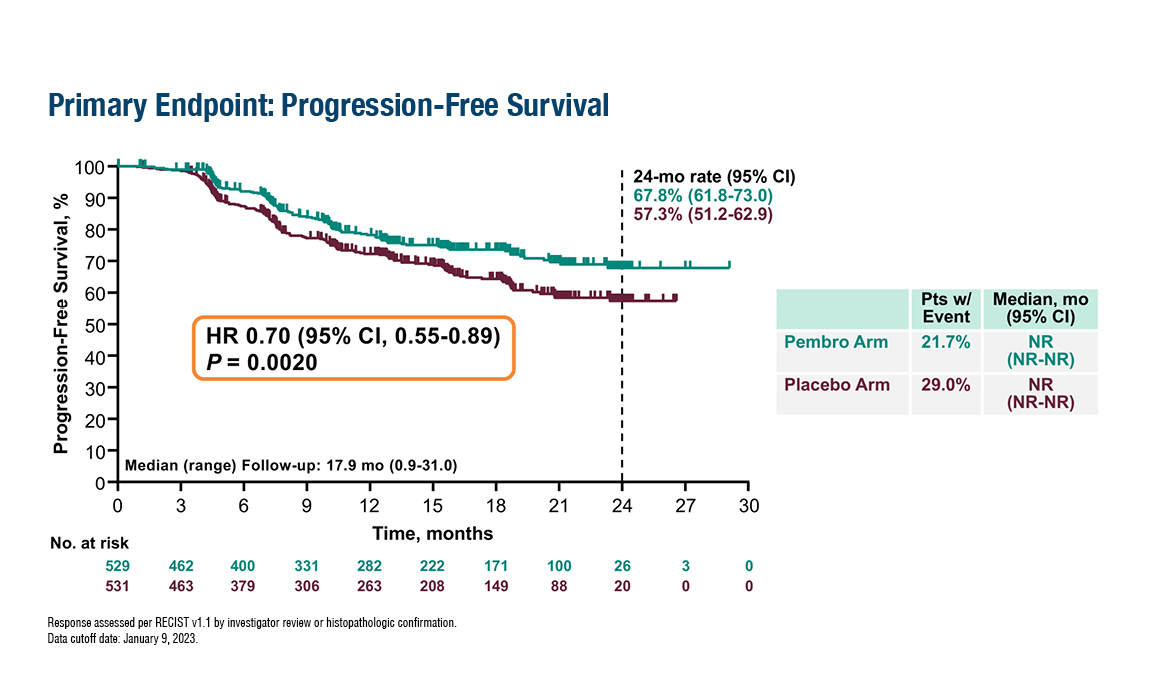
j
より引用
いよいよ子宮頸がんの初回治療に免疫チェックポイント阻害薬が入ってくるんですね!
参考文献:

