さ~て、先日、ある資料を読んでいましたら『塩化ナトリウム型構造』と言うモノに久し振りで出会いました。
今日は、小職の復習の意も込めて『塩化ナトリウム型構造』を見て参ります。
尚、『化学のグルメ』の公式ホームページに掲載されたモノを転載させて頂きます。
塩化ナトリウム型構造とは
下図のような構造をもつイオン結晶を塩化ナトリウム型構造(NaCl型構造)という。
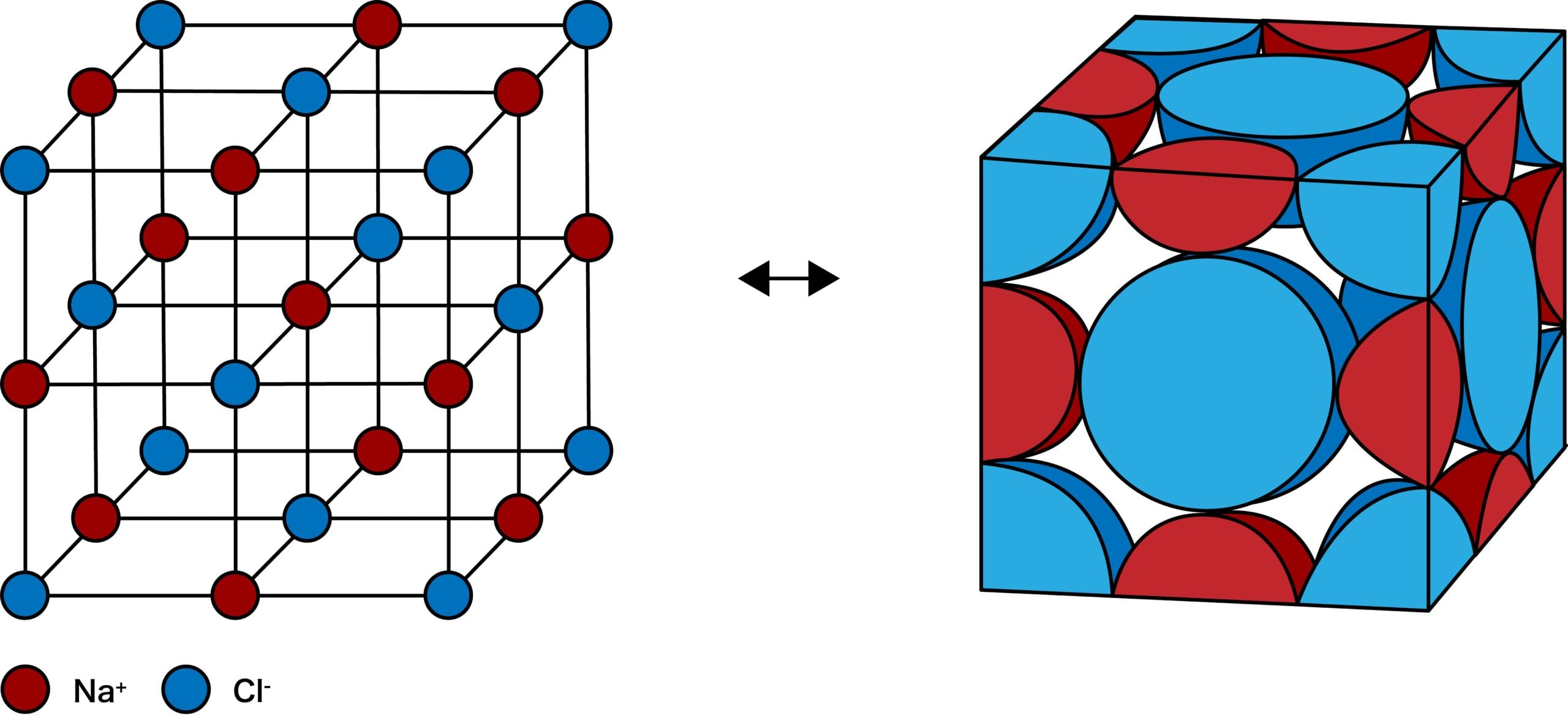
塩化ナトリウム型構造に含まれる陽イオン・陰イオンの数
Na+の数
4コ
Point!
まずは、塩化ナトリウム型構造(NaCl型構造)に含まれるNa+を数えていこう。
塩化ナトリウム型構造(NaCl型構造)に含まれるNa+のうち、格子の各“辺”にあるものはNa+を4分割した状態になっている。
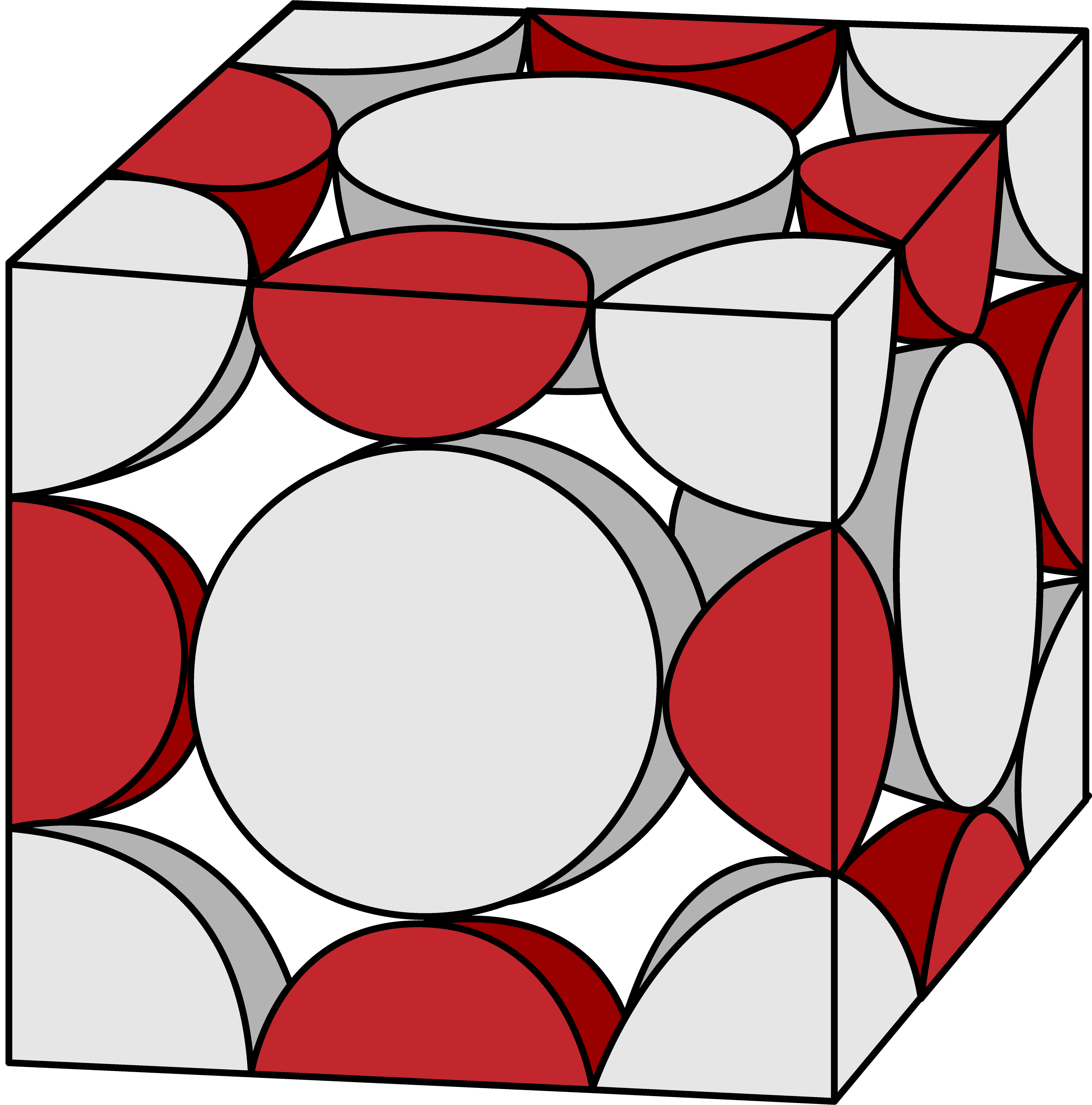
したがって、4分割(1/4)したものが辺の数分=12コあるので…
14×12=314×12=3
辺にあるNa+の数は合わせて3コである。
また、塩化ナトリウム型構造(NaCl型構造)に含まれるNa+のうち、格子の中心にあるものは丸々1コである。
以上より、塩化ナトリウム型構造(NaCl型構造)に含まれるNa+の数は…
3+1=43+1=4
4コである。
Cl–の数
4コ
Point!
次に、塩化ナトリウム型構造(NaCl型構造)に含まれるCl–を数えていこう。
塩化ナトリウム型構造(NaCl型構造)に含まれるCl–のうち、格子の各頂点にあるものはCl–を8分割した状態になっている。
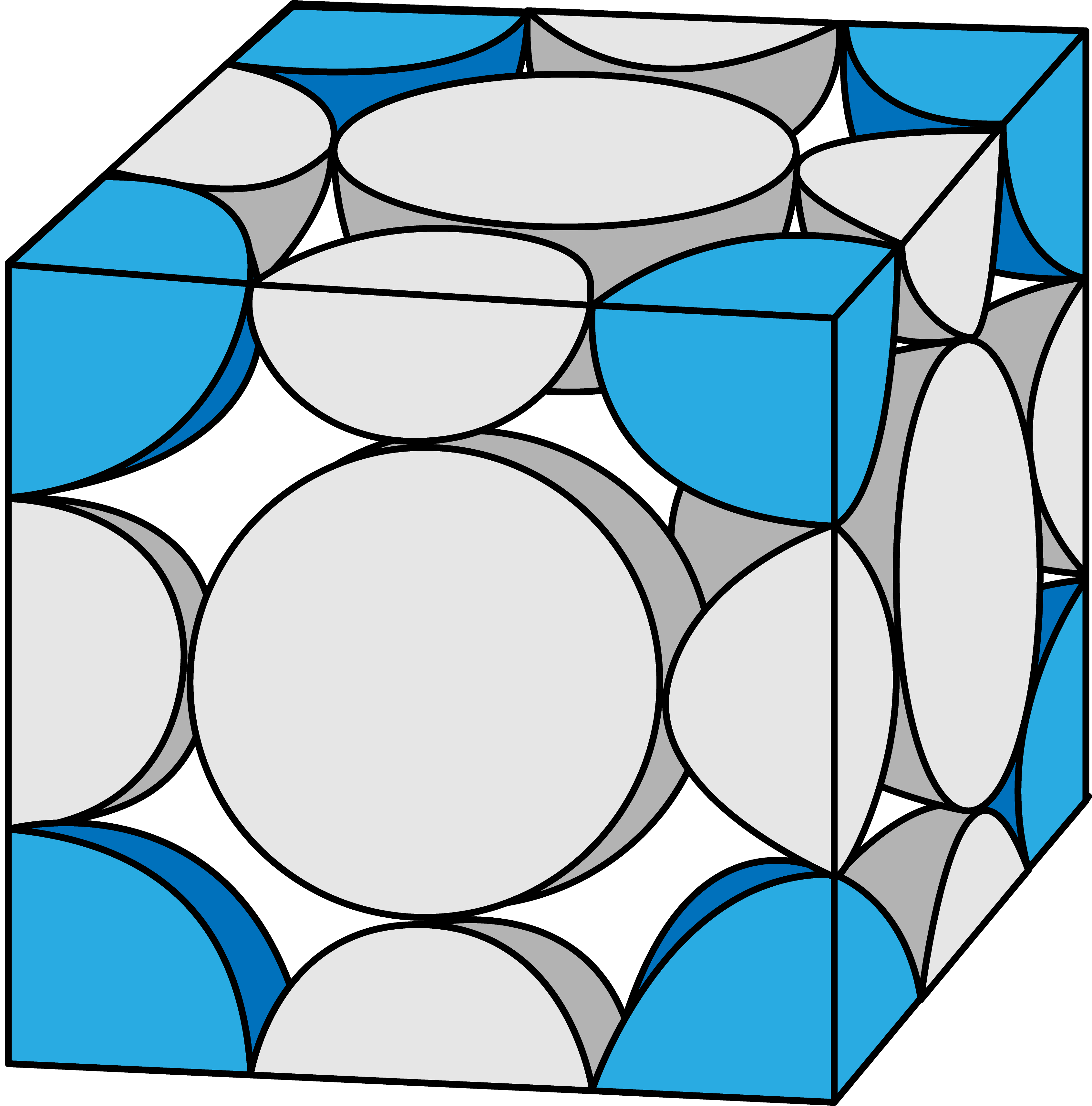
したがって、8分割(1/8)したものが頂点の数分=8コあるので…
18×8=118×8=1
頂点にあるCl–の数は合わせて1コである。
塩化ナトリウム型構造(NaCl型構造)に含まれるCl–のうち、各“面”の中心にあるものは、Cl–を2分割したものになっている。
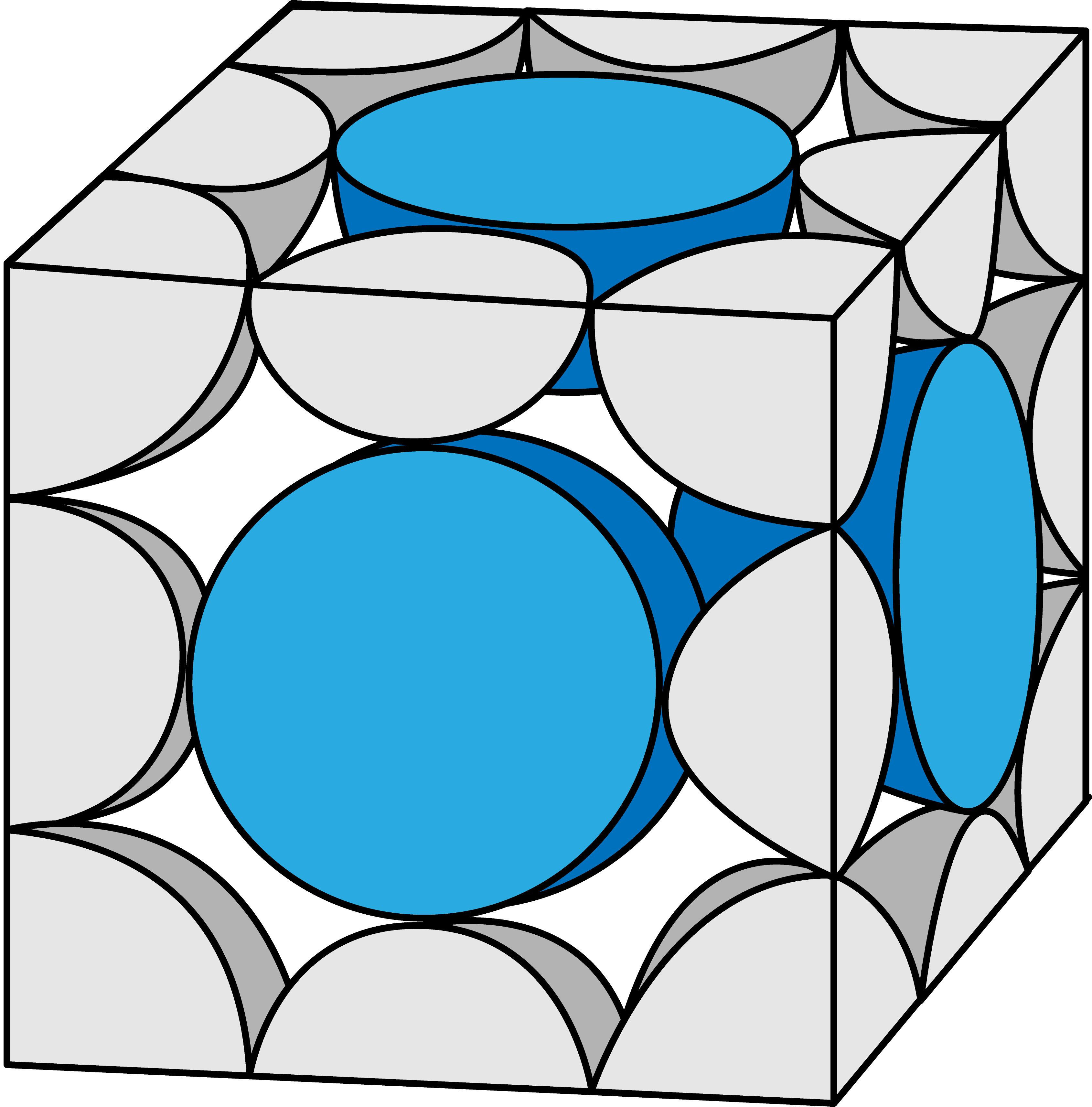
したがって、2分割(1/2)したものが面の数分=6コあるので…
12×6=312×6=3
面の中心にあるCl–の数は合わせて3コである。
以上より、塩化ナトリウム型構造(NaCl型構造)に含まれるCl–の数は…
1+3=41+3=4
4コである。
塩化ナトリウム型構造の配位数
6コ
Point!
塩化ナトリウム型構造(NaCl型構造)では、中心のNa+は周りの6コのCl–と接しており、同様にCl–も周りの6コのNa+と接している。
したがって、塩化ナトリウム型構造(NaCl型構造)の各イオンの配位数は6となる。
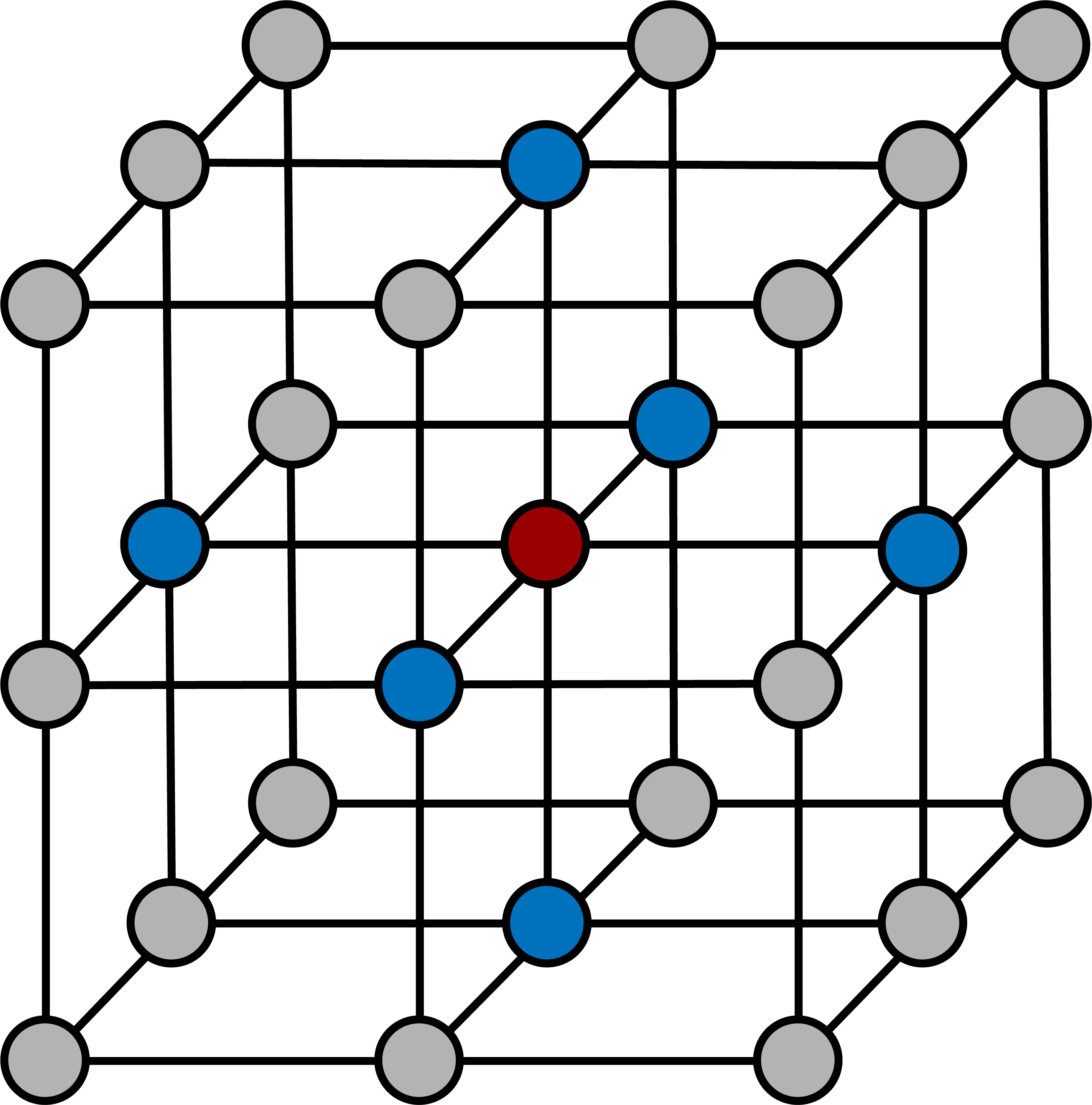
塩化ナトリウム型構造のイオン半径と単位格子一辺の長さとの関係
a=2(rNa+ + rCl–)
Point!
Na+・Cl–のイオン半径をそれぞれrNa+・rCl–、単位格子一辺の長さをaとし、塩化ナトリウム型構造(NaCl型構造)の面の部分に注目すると…
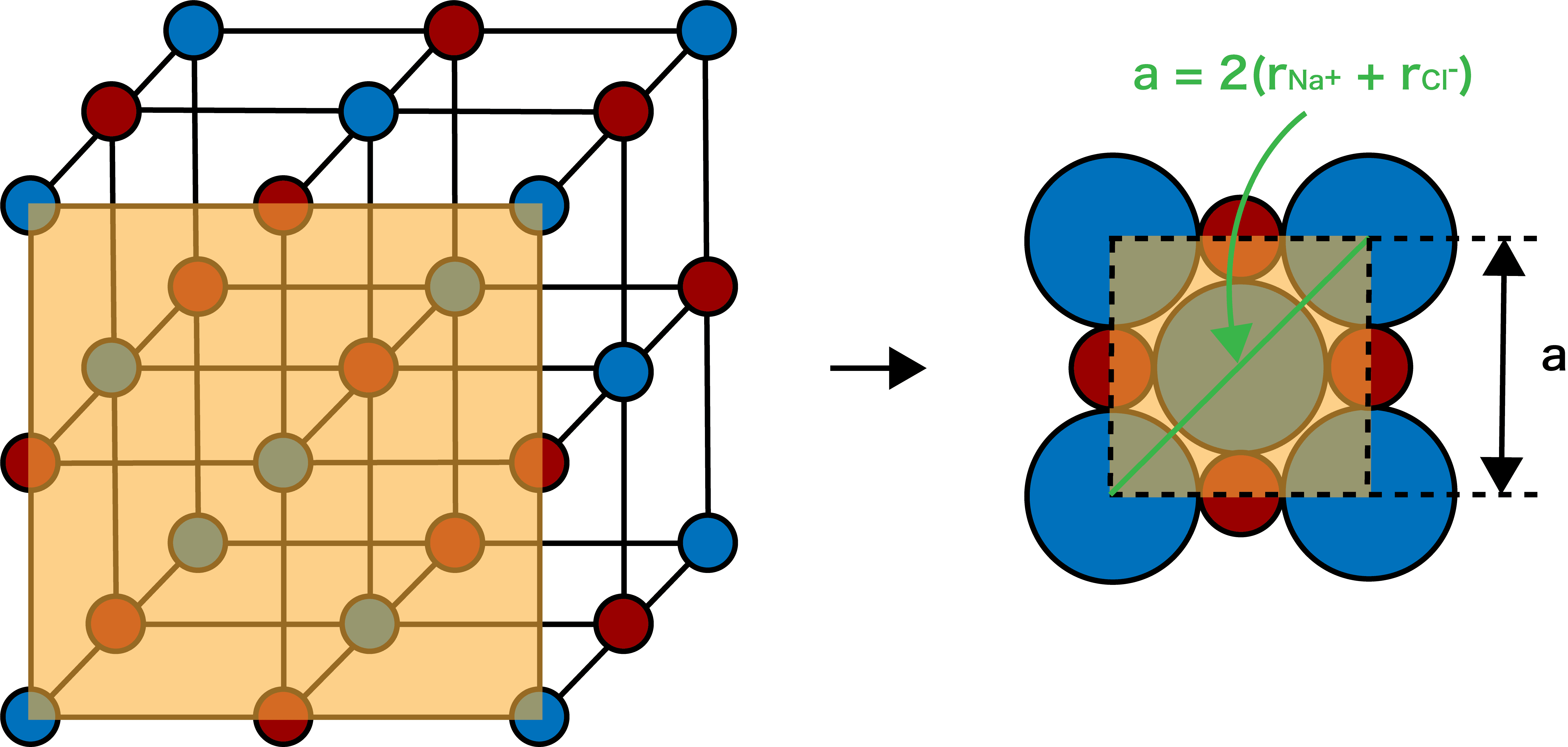
a=2(rNa++rCl−)a=2(rNa++rCl−)
イオン半径と単位格子一辺の長さの間にこのような関係があることがわかる。
塩化ナトリウム型構造の限界半径比
0.41~0.73
Point!
塩化ナトリウム型構造(NaCl型構造)の限界半径比は0.41〜0.73である。
※限界半径比について詳しくは「限界イオン半径比(定義・求め方・配位数との関係など)」を参照
塩化ナトリウム型構造に関する演習問題
問1
【】に当てはまる用語を答えよ。
下図のような構造をもつイオン結晶を【1】という。

【問1】解答/解説:タップで表示

問2
【】に当てはまる用語を答えよ。
塩化ナトリウム型構造に含まれるNa+の数は【1】コである。
【問2】解答/解説:タップで表示

14×12=314×12=3
3+1=43+1=4
問3
【】に当てはまる用語を答えよ。
塩化ナトリウム型構造に含まれるCl–の数は【1】コである。
【問3】解答/解説:タップで表示

18×8=118×8=1

12×6=312×6=3
1+3=41+3=4
問4
【】に当てはまる用語を答えよ。
塩化ナトリウム型構造の配位数は【1】である。
【問4】解答/解説:タップで表示

問5
【】に当てはまる用語を答えよ。
塩化ナトリウム型構造のナトリウムイオンNa+半径、塩化物イオンCl–半径、単位格子一辺の長さの関係を式で表すと【1】となる。
【問5】解答/解説:タップで表示
a=2(rNa++rCl−)a=2(rNa++rCl−)

a=2(rNa++rCl−)a=2(rNa++rCl−)
問6
【】に当てはまる用語を答えよ。
塩化ナトリウム型構造の限界イオン半径比は【1】〜【2】である。
と言う事でした。なかなか、素晴らしい記述内容でした。
では、本日の小職の予定です。
今日は、多くの時間、収益法人事案(NPO法人事案を含む)に伍します。
ただ、朝夕は、社会福祉法人に参ります。