カテゴリ:◆母・いろいろ
【国内初】
ロート製薬が新型コロナ治療薬の治験を
8月メドに開始予定。
再生医療で重症肺炎の治療目指す
6/24(水) 20:00配信
ロート製薬は6月23日、新型コロナウイルス感染症(COVID-19)の重症者を対象に、早ければ8月から「他家間葉系幹細胞」を用いた再生医療の企業治験を開始する予定だと発表した。
【全画像をみる】【国内初】ロート製薬が新型コロナ治療薬の治験を8月メドに開始予定。再生医療で重症肺炎の治療目指す
この治験では、同社が肝硬変の患者に対する治療薬として開発を進めている細胞製剤「ADR- 001」の適応を拡大することで、COVID-19の重症肺炎患者の治療薬として活用することを目指しているという。
再生医療として期待の「間葉系幹細胞」とは?
間葉系細胞(MSC)とは、さまざまな細胞に変化(分化)できるiPS細胞やES細胞などと同じ「幹細胞」の一種。iPS細胞などほどに分化能力は高くはないが、長年研究が続けられてきた細胞だ。
「他家間葉系幹細胞」の「他家」とは、「他の人」という意味。
つまり、今回使用する治療薬は、他の人の体由来のMSCを培養して薬にしたものだ。
実は現在、COVID-19用の治療にMSCを用いた治療薬が有効ではないかとして、世界各国で研究が進められている。
ロート製薬会長の山田邦雄氏は、今回の治験の経緯について、
「ロート製薬は、(脂肪由来)間葉系幹細胞の研究を重ねてきました。現在、肝硬変の治療薬として治験が行われているところです(安全性質に関する治験は終了)。幸い、確立された(間葉系)幹細胞が準備できておりますし、(COVID-19に対して)役に立てないかということで今回の治験を企画するに至りました」
と話した。
8月~12月に治験予定。承認メドは「結果次第」
今回の治験対象となるのは、COVID-19によって肺炎が重症化した患者。
治験では6人の患者に対して、1カ月(4週間)にわたり、同社が開発した治療薬を1週間に1度の頻度で静脈に点滴で投与する予定だ。
その後、2カ月程度の経過観察期間を経て、まずは安全性について評価することを目指すとしている。
ただし、治験対象者がCOVID-19の重症者であることから、ロート製薬臨床研究グループマネージャーの高尾幸成氏は、
「あくまでも安全性をメインにした試験をさせていただきたいと思っています。ただし、患者様に投与するということから、初期の薬効評価という形で、どのような有効性を示すのかを探索的に調べさせていただく治験です」
と話す。
治験の具体的な日程はまだ明らかになってはいないが、6月中には申請を済ませ、2020年8月~12月にかけて実施したいとしている。
なお、実際に治療薬として承認される時期については、「臨床試験の結果次第」という表現に留められた。
早期承認制度などの枠組みを利用して治療薬としての認証を得ようとする試みについても、記者会見では明らかにされなかった。
MSCの効果、副作用は?
また、記者会見では、大阪大学大学院医学系研究科の澤芳樹教授から、MSCを用いたCOVID-19の治療薬の効果についてもレクチャーがあった。
COVID-19による肺炎の重症化は、免疫細胞のはたらきが制御できなくなる「サイトカインストーム」という現象によって引き起こされていると考えられている。
この現象が起きると、肺が過剰に炎症を起こし、その結果、ECMO(エクモ、体外式膜型人工肺)や人工呼吸器と言った装置を使用せざるを得ないほど、状態が悪化してしまうのだ。
「インフルエンザウイルスでも、重症化すると肺炎が起こります。ただし、免疫が適正にはたらけば、軽症の肺炎でリカバリーできます。COVID-19の場合は、免疫機能が崩壊につながるような重症化をもたらす患者さんがいらっしゃいます。(この現象は)COVID-19に限った話ではないのですが、(新型コロナウイルスは)こういった病態を起こしやすいウイルスだといえます」
と、澤教授は話す。
ロート製薬が事前に実施した細胞の培養器内での予備実験では、MSCを使うことで、免疫細胞からの炎症物質の放出を抑える効果を期待できる結果が得られているという。
今回の治験では、治療薬が静脈から点滴によって投与される予定だ。
治療薬に含まれるMSCは、血流に乗って肺付近に到達し、そこである程度が留まると想定される。
澤教授は、
「ばらばらと細胞が肺にトラップされると、免疫抑制効果がある物質をたくさん分泌するのではないかと思います。これがARDS(肺炎などによる重度の呼吸不全)を抑えると期待されています」
と、治療薬の効果について期待を話す。
国内ですでに承認されている治療薬「レムデシビル」や、効果が期待されている「アビガン」などは「抗ウイルス薬」。基本的に、ウイルスの増殖を防ぐことを目的としているため、肺の炎症を抑制する効果はあまり期待できない。
そういった意味でも、重症化した肺炎を治療できる可能性をもつ治療薬の登場は、今後も続くであろう新型コロナウイルスとの闘いにおいて非常に重要だといえる。
なお、「現時点で想定されている副作用は何か?」という、Business Insider Japanからの質問に対して、ロート製薬からは以下のような回答があった。
「現状、重篤な有害事象は確認されておりません。一般的に細胞の静脈投与の懸念は肺塞栓(肺の血管が詰まってしまう現象)になりますが、動物試験から安全域を設けておりますので、本治験の投与量では発生しないよう設定しております。COVID-19の患者様特有の安全性にかかる問題もあろうかと思われますので、本治験で確認したいと思っております」
少なくとも、肝硬変の治療薬としての安全性に関する治験において、問題がないという結果が得られていることから、薬としての基本的な安全性は満たしていると考えられるだろう。ただし、対象疾患が変われば、それに応じて安全性を確かめなおす必要がある。
今回の治験は、まさにその試験の場と言える。
未承認薬による治療に警鐘。科学的エビデンスのある治療薬に期待
間葉系幹細胞(MSC)をCOVID-19を対象に投与する治験は、今回のロート製薬の取り組みが日本では初のものになる。
つまり、COVID-19の治療を目的として薬事承認された「幹細胞を用いた治療薬」は、現時点において少なくとも国内では存在しない。
実は6月4日、学術誌「Cell Stem Cell」に、一部の企業がCOVID-19に対する「幹細胞治療」「予防療法」などと称して、科学的に効果が検証されていない治療薬を提供しようとしていることを批判する論説が掲載された。
記者会見でも、澤教授から「自由診療でこういったことをやられている人がいらっしゃる」との発言もみられた。
未承認の薬の使用は、効果があるかどうか分からないばかりか、逆に患者を危険にさらすことにもつながりかねない。
また、COVID-19に対する治療薬の開発でも、迅速性が求められるあまり、科学的な検証が不十分になる可能性が度々懸念されてきた。
こういった懸念を払拭するためにも、治験によってしっかりとした科学的なエビデンスの担保された治療薬の登場が期待されるところだ。
一方、薬の開発にはそれなりに時間がかかるのも事実だ。
開発が完了する頃には、すでに感染症の流行が収束していたり、ワクチンができたりしている可能性もある。
COVID-19では重症患者数も限られていることから、製薬企業にとって、感染症の治療薬の開発に取り組むことは、ビジネスとして一定のリスクのある選択だともいえる。
この点について、ロート製薬の山田会長は、次のような製薬企業としての社会的責任に関する見解を述べて、会見を締めくくった。
「当初、感染症(に対する治療薬の開発)の優先順位を落としていました。ただ、世界をみればまだまだ猛威を奮っています。また、新型コロナウイルスではないウイルスが出てくるかもしれません。そういったときに、肺の症状というのは心配されるわけです。急ぎたい気持ちもあるが、将来を考えれば着々と準備をしておき、いざというときに役に立てるような種を育てておくことは、有意義ではあるだろうと思います」
(文・三ツ村崇志)
三ツ村 崇志
★8月から治験
ということは、順調にいけば
来年承認、ということになるかな?
今、日本では感染者数が減少しているので
アビガンも苦労しているし、、、
新型コロナウイルス特効薬候補アビガン関係
⇓

2020.06.03
「アビガン」のジェネリック
ロシアが新型コロナ薬として暫定承認
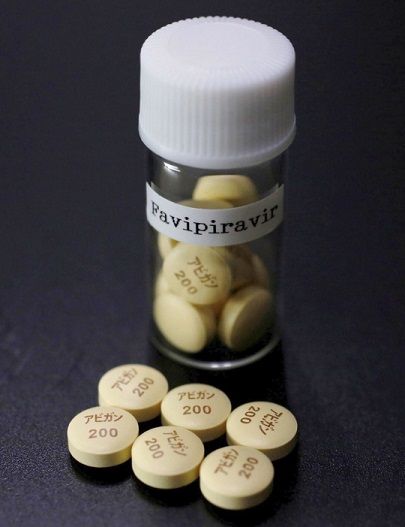
アビガンの5月承認を断念
効果まだ不明、企業未申請
5/25(月) 22:54配信
新型コロナウイルス感染症の治療薬候補アビガンを巡り、安倍晋三首相が目指すとした「5月中の承認」を政府が断念したことが25日、分かった。25日時点で審査の前提となる企業からの承認申請はなく、月内に審査を終えるのは不可能と判断した。政府関係者が明らかにした。
【写真】アビガン「7日以内に7割が回復」
国内では承認を目指して企業による治験が進んでいるほか、国には大学による臨床研究の結果を承認審査に活用したいとの考えもある。しかし現段階では、有効性を示すデータが出ておらず、手続きが進むのは6月以降になる見通し。
首相は5月4日の記者会見で「有効性が確認されれば今月中の承認を目指したい」と表明していた。
関連1
⇓
◆富士フイルムHD株反落、
アビガン有効性示せずとの報道-
デンカも安い
5/20(水) 9:43配信
(ブルームバーグ): 20日の東京株式市場で、富士フイルムホールディングスの株価が一時4.9%安の4818円と4月9日以来の日中下落率となった。新型コロナウイルス感染症治療薬としての承認が期待される「アビガン」の臨床研究で明確な有効性が示されていないと、共同通信などが報じたことがきっかけとみられている。
.
シティグループ証券の芝野正紘アナリストらは英文メモで、アビガンの早期申請には賛否両論あり、「有効性が認められるのに時間がかかった場合は株価にネガティブになる」と指摘している。一方で、ゲイツ財団などのプロジェクトから新型コロナ治療薬の製造を受託したと4月末に発表したことなど評価できる点も同社にはあるという。
.
原料の製造などで注目されていたデンカが一時5.9%安、カネカも同2.7%安と売られている。
.
(c)2020 Bloomberg L.P.
Ayaka Maki, Aoi Fujimoto
◆富士フイルム、
今年度内にアビガン200万人分の納品完了予定
5/22(金) 15:34配信
[東京 22日 ロイター] - 富士フイルムホールディングス<4901.T>は22日のオンライン決算会見で、新型コロナウイルス治療薬候補「アビガン」について、政府の追加備蓄要請である200万人分の納品を2020年度内に完了する予定だと発表した。現時点で約70万人分の備蓄がある。4月から増産を開始しており、今後、段階的に生産能力の向上を目指す。
「アビガン」は富士フイルム富山化学が開発した新型インフルエンザの治療薬。日本医師会の有識者会議は18日、同治療薬の明確な有効性は示されていないと発表し、科学的根拠が十分でない候補薬を承認すべきではないと懸念を示した。
富士フイルムの岡田淳二・取締役医薬品事業部長は「臨床試験で新型コロナに対するアビガン錠の有効性と安全性を確認することで治療薬としての承認取得を進めていく」と述べた。具体的な承認の申請時期については「今まさに規制当局と調整、協議している段階。いつ頃かは控えさせていただきたい」と語った。
同時に発表した2020年3月期(前期)の純利益(米国基準)は、前年比9.5%減の1250億円だった。売上高は同4.8%減の2兆3151億円、営業利益は同11.1減の1866億円となった。
部門別にみると、「ヘルスケア&マテリアルズ」部門の営業利益は、同5.3%減。新型コロナ感染拡大を受け回診用X線撮影装置などの販売は伸長したものの、病院への営業活動自粛や商談の遅延が発生した。「イメージングソリューション」部門は、新型コロナの影響による中国工場の稼働率低下や小売店の休業により、同51%減と大幅に落ち込んだ。
期末配当は、従来の予想通り47円50銭とした。
21年3月期(今期)の業績・配当予想は未定とした。新型コロナが世界規模で拡大している影響により、現時点で合理的な算出が困難であるため。
リフィニティブがまとめたアナリスト12人による純利益予想の平均は1666億円となっている。
*内容を追加しました。
(新田裕貴 編集:内田慎一)
関連2
⇓
◆悪化前にもアビガン投与可
現場判断で、福岡県医師会
2020年5月12日 10:33
福岡県医師会は11日、記者会見し、新型コロナウイルス感染症の治療薬として期待されるインフルエンザ治療薬アビガンを、症状悪化前でも現場医師の判断で投与できる運用を始めたと明らかにした。
◆悪化前でもアビガン投与可、
現場判断で 福岡県医師会
福岡 2020/5/11 20:24
(2020/5/11 22:01更新)
福岡県医師会は11日の記者会見で、新型コロナウイルスの治療薬として期待されるインフルエンザ治療薬アビガンを、症状悪化前でも現場医師の判断で投与できる運用を始めたことを明らかにした。厚生労働省の通知に基づく「観察研究」として行い、県医師会が認めた医療機関で実施する。
厚労省は患者が同意し、医師が必要と判断した場合に限り、観察研究としてアビガンの使用を認めている。4日には「倫理委員会の承認は投与開始後、事後でも差し支えない」と都道府県に通知しており、医師会の運用はこれを受けたもの。
福岡県の新型コロナ対策の担当者は「症状悪化前でもアビガン投与が認められるのは珍しいのではないか」と話している。
国はアビガンについて、5月中の薬事承認を目指している。投与には各医療機関の倫理委員会を経て、臨床研究を進める藤田医科大(愛知県)や厚労省に申請する必要がある。
医師会によると、新たな運用は高齢者や、基礎疾患があって重症化の恐れがある患者に現場医師の判断でアビガンを投与でき、その後に医師会の倫理委に報告すればよいとしている。
医師会の上野道雄副会長は、これまでは症状が悪化した後の投与が中心だったと指摘。「(新たな運用で)投与できる患者はかなりの数になるだろう」と話した。
〔共同〕
◆アビガン投与「福岡県方式」構築
47機関、医師判断で早期対応可能に
|【西日本新聞ニュース】
2020/5/11 21:20 (2020/5/11 21:26 更新)
西日本新聞 井上 真由美
福岡県医師会は11日、新型コロナウイルス感染症への効果が期待される新型インフルエンザ治療薬「アビガン」を、主治医が重症化の恐れがあるなどと判断した場合、軽症でも早期投与できる独自の体制を整えたと発表した。県内47の医療機関が参加を表明しており、県医師会は「『福岡県方式』の構築で新たに投与できる患者はかなり多く、影響は大きい」としている。
【関連】アビガン投与、現場の医師判断で 県医師会が「福岡県方式」検討
アビガン投与には、藤田医科大(愛知)などの観察研究への参加が必要。県医師会が一括して必要な手続きを行ったことで、これまで未参加だった27機関が加わり、計47機関で投与できるようになった。今後も増える見通し。
主に重症や中等症の患者に投与されていたが、「主治医等が重症化の可能性を憂慮する患者」を対象に明記したことで、主治医が必要と判断すれば軽症でも早期投与が可能としている。投与には入院が必要という。
ただ、アビガンは動物実験で胎児に奇形が出る恐れが指摘され、妊婦や妊娠の可能性がある人などには使えない。肝機能障害などの副作用も報告されており、患者への十分な説明と同意が必要となる。
新型コロナ感染症の治療薬としては、厚生労働省が7日、米製薬会社が開発した「レムデシビル」を国内で初承認。安倍晋三首相はアビガンについても今月中に承認する意向を示している。(井上真由美)
★

2020.05.20
「臨床研究や治験の結果を待つ」
アビガン巡り厚労相

アビガン「有効性示せず」
ってどういうこと?
期待は裏切られたのか、
専門家に聞きました:新型コロナ
市川衛 | 医療の「翻訳家」
◆アビガン「有効性示されず」報道は誤解
藤田医科大が見解
2020/05/20 19:40

2020.05.03
富士フイルムが天下りを受け入れないから?
アビガン認可8月になる見通し問題
年内、なんて悠長な話しもあるよ。
死ななくていい人たちが
それじゃあ、全員死んじゃってるよ

「アビガン」は
新型コロナに本当に効くのか?
開発者に聞いた
4/19(日) 11:02配信
(FRIDAY) - Yahoo!ニュース
COVID-19は現在、生死がかかった病気と思われていますが、早期発見してアビガンを飲めば、肺炎がそれ以上進行しない病気だという安心感をみなさんに持ってほしいですね
画像はアビガンを富士フイルム富山化学と共同開発した、
富山大学医学部名誉教授で千里金蘭大学副学長の白木公康氏
◆2020.05.04
首相 アビガンの月内承認指示
◆富士フイルムのグループ会社が開発した
新型インフルエンザ薬「アビガン」の有効性を
臨床試験で確認:中国科学技術省
◆2020.04.03
アビガン無償提供?
◆中国など外資の新薬買収防止策など
、、、アビガンについて
◆アビガン認可に抵抗した厚労医官、
今井秘書官は経産省にアビガン推進チーム
◆2020/05/11(月)21:18
治療薬候補「アビガン」、
医師判断で軽症者にも早期投与可能に
福岡県医師会
◆2020.05.02
赤江珠緒がアビガンで改善
投与可否の理由明かす
◆2020.04.20
クドカン、発症~治療の経緯を詳細に語る
「最初は背中が痛くて…」
入院後高熱でアビガン投与
★
★★