レプリコンmRNAワクチン:日本が世界初の自己増幅mRNAワクチンを承認
新たな悪夢が市場に登場する。今は何ですか?問題点は何ですか? 脱皮についてはどうですか?
2023年11月27日– 日本の厚生労働省、成人向けの新型コロナウイルス感染症に対して承認された初の自己増幅型mRNAワクチンであるCSLとArcturus TherapeuticsのARCT-154を承認
- 「世界初の自己増幅メッセンジャーRNA(sa-mRNA)新型コロナウイルスワクチンの歴史的な承認」
- CSLとArcturus Therapeuticsは、日本の厚生労働省(MHLW)が、18歳以上の成人を対象とした初回ワクチンおよび追加接種用の自己増幅型mRNA(sa-mRNA)新型コロナウイルス感染症ワクチンARCT-154の承認を与えたと発表した。
- ノーベル賞受賞者のドリュー・ワイズマン博士は、「自己増幅mRNA技術は、永続的なワクチンの選択肢となる可能性を秘めています。この次世代mRNA技術が多くの人を新型コロナウイルス感染症やおそらく他の有害な感染症から守ることを楽しみにしています。」と語った。
- この承認は、ベトナムで実施されている16,000人の被験者を対象とした有効性試験や 、新型コロナウイルス感染症(COVID-19)ブースター試験の第3相試験を含む、いくつかのARCT-154試験から得られた肯定的な臨床データに基づいている。標準 mRNA COVID-19 ワクチン比較ツール。最初の研究結果はMedRxivに掲載されており 、年末までに査読付き雑誌に掲載される予定です。
- 世界最大のインフルエンザワクチンプロバイダーであるCSLのワクチン事業であるCSL Seqirusは、sa-mRNA 新型コロナウイルスワクチンARCT 154の日本での販売に関してMeiji Seika ファルマと独占的に提携した。
- Arcturus Therapeutics (カリフォルニア州サンディエゴ) の最高経営責任者、Joseph Payne 氏は次のように述べています。
自己増幅型 mRNA ワクチンとは何ですか?
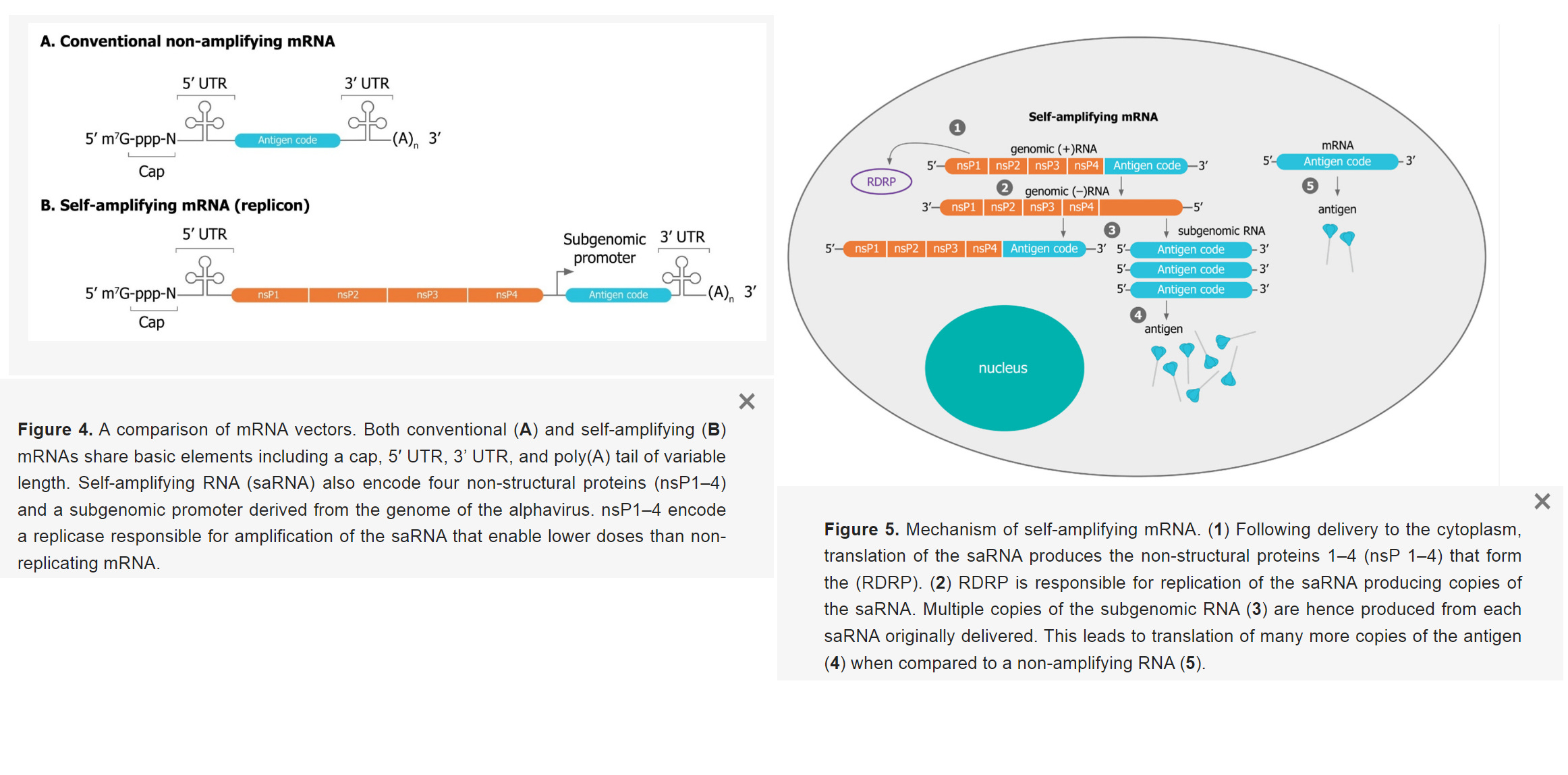
- 「レプリコンは、標的細胞に投与された直後にコピー数を増加させるために、独自の複製機構をコード化します。」
- 「レプリコン RNA はさらに、ウイルス レプリカーゼ遺伝子をコードします。これらの遺伝子により、mRNA の迅速な増幅が可能になります。自己増幅ウイルス遺伝子は、アルファウイルスやフラビウイルスなどのウイルスに由来します。」
16センターベトナム「安全調査」日本政府が承認に利用
- ワクチン: 「ARCT-154 は、ウイルス構造タンパク質をコードする RNA が SARS-CoV-2 D614G ウイルスの全長スパイク (S) 糖タンパク質をコードする RNA に置き換えられたベネズエラ馬脳炎ウイルスに基づくレプリコンで構成されています」 、単一の点突然変異を含む祖先株の初期の変異体であり、脂質ナノ粒子にカプセル化されています。有効成分 100 μg をバイアルに入れて -20℃ 以下で保存し、使用直前に 10 mL の滅菌生理食塩水に溶解し、5 μg を含む 0.5 mL を三角筋に筋肉注射して投与しました。」
- 「宿主細胞がワクチンのmRNAのコピーを作ることを可能にし、より少ない用量のmRNAの投与で生成されるタンパク質の量を増加させる」
- 「加速承認」 = 当社は、ARCT-154 の安全性、反応原性、免疫原性、および有効性を評価するために、EMA、FDA、および WHO のガイダンスに従って設計された現在の加速統合第 1/2/3a/3b 相試験を開始しました。
- 私たちは、この新しいワクチンを人間のボランティアに最初にワクチン接種してから最大 3 か月後の最初の研究結果を発表します。
- 90%が初回投与後に少なくとも1つの有害事象を経験した(最も軽度)
- 「全体的な全身性AEと局所反応は、認可されたmRNAワクチンよりもARCT-154の接種者では頻度が低かった。」
- 「日本での並行研究では、一次ワクチンとして主にBNT162b2であるmRNAワクチンで完全に免疫を受けた成人において、中和抗体として測定した場合、追加用量のARCT-154に対する免疫応答が追加用量のBNT162b2に対する免疫応答よりも優れていることが示されました」 」
- 「ARCT-154は、循環している変異株に対する免疫レベルを強化し、拡大するための一次免疫ではなく追加免疫として使用される可能性が最も高いです。」
小田らによる2023年12月20日の日本研究
- 18歳から64歳までの828人の参加者が登録した。
- 3x mRNA ワクチン接種者(ファイザーまたはモデルナ)には、ARCT-154 またはファイザーのいずれかの 4 回目のブースターショットが投与されました。
- ARCT-154の注射後28日目ではファイザーと比較して免疫反応が良好
- 「どちらのブースターも同様に忍容性が良好でした」
Lowらによる2022年12月13日の研究
- ボランティア 169 名、フェーズ I/II
- ARCT-021 は、7.5 μg の用量までは一般に良好な耐容性を示しました。
- 10μgの用量は、グレード3の重症度を含む、より局所的および全身的な誘発性AEと関連していた
- グレード 2 以上のリンパ球減少症には用量関連傾向があるようで、1.0、3.0、5.0、7.5、10 μg の用量レベルでそれぞれ影響を受けた参加者の 0%、25%、26.5%、30.0%、および 40.0% でした。 。リンパ球減少症の発症は注射後 24 時間以内に起こり、通常は 1 日以内に何事もなく解消されました。
メリット"
- ARCT-154 (5 μg) は、他の RNA ベースの COVID-19 ブースターと比較して、1 人あたりのワクチン必要量が 10 分の 1 ~ 6 分の 1 です。
- 1回の注射で投与されるワクチンの量を減らすと「生産コストが下がる」はずです
- saRNA はウイルスに似た性質を持っているため、独特の方法で免疫系と相互作用します。
- ARCT-154 の承認が日本で確保されたことを受けて、その開発者は現在ヨーロッパでの承認を求めています。来年には規制当局の決定が下される予定だ。
- 昨年8月、流行対策イノベーション連合(CEPI )は 、自己増幅型saRNAプラットフォームの開発に最大360万ドルを提供すると発表した。
- 「一度投与すると、これらの分子の発現は長期間持続します。」したがって、企業は、患者の線量負担を軽減しながら、より少ない量を製造することでコストを節約することが期待できます。用量が少ないほど、潜在的な副作用も少なくなる可能性があります。
- RNA ワクチン候補の生産は速く、インフルエンザ ワクチン候補はわずか 8 日で生産されたと報告されています [8]。
- 「mRNA が宿主ゲノムに組み込まれるリスクはありません [9]。mRNA は非感染性であり、宿主細胞の RNase による分解により細胞内に一時的にのみ存在します。」
- 「sa-mRNAワクチンは持続的な新型コロナウイルス感染症の予防接種を促進する」
- ワクチン接種後12か月間、免疫反応の上昇を維持する
問題点"
- Arcturus は独自の「脂質ナノ粒子」を使用– 詳細はあまり入手できませんが、ファイザーとモデルナの LNP に似ていると主張しています
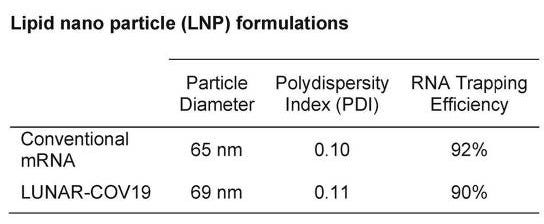
- Arcturus LNP については、安全性研究や生体内分布研究は利用できません。
- sa-mRNA は、(追加の複製機構配列により) 最大 3 倍も大きくなります。
- 欠陥のあるsa-mRNAは注入されると細胞内で増幅され、欠陥タンパク質の濃度が高くなります。
- ほとんどの saRNA ワクチンは、ポジティブセンス アルファウイルス、ベネズエラ馬脳炎ウイルス (VEEV)、シンドビス ウイルス (SINV)、またはセムリキ森林ウイルス (SFV) のゲノムに基づいています (以下を参照)。
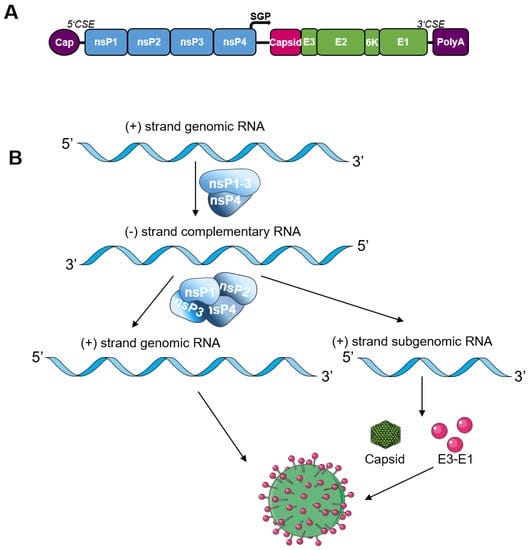
- saRNA ワクチンの構築では、アルファウイルスの構造タンパク質が抗原遺伝子 (新型コロナウイルス感染症ワクチンのスパイクタンパク質) に置き換えられます。
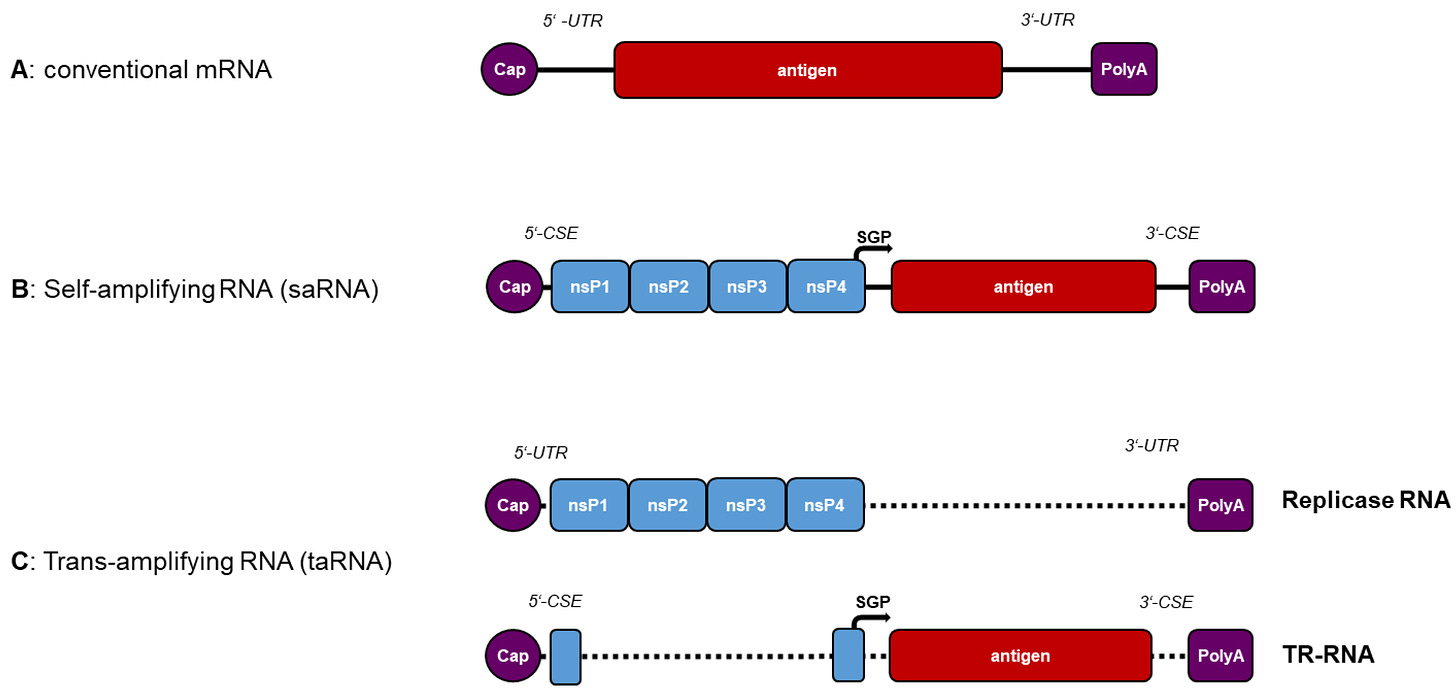
- どれだけの「増幅されたmRNA」が生成されているかの指標はありません
- どれだけのスパイクプロテインを生成しているかはわかりません
- ウイルスレプリカーゼは、まずポジティブセンスゲノムを鋳型として使用して、相補的なネガティブセンスRNAを合成し、その後、ゲノムおよびサブゲノムプラス鎖RNAの合成の鋳型として機能します。
- 「RNA増幅と抗原発現がどのくらいの期間続くのかを解明する必要は依然としてある[ 70 ]。
- DNA汚染?はい、お願いします
- 「saRNA と taRNA は、mRNA と同様に、インビトロ転写とキャップ構造の付加によって DNA 鋳型から生成されます。」
- 「自然免疫の活性化を回避するためのいくつかのアプローチが適用できます。ただし、sa/taRNA ワクチンの場合、ヌクレオシド修飾は増幅ステップ中に失われるため、利点は少なくなります。」
- mRNA ワクチンとは対照的に、細胞内 RNA の増幅により dsRNA が生成され、自然免疫応答がより強力に活性化されます。RNA は、TLR3、TLR7 などの複数のパターン認識受容体によって認識されます。
- LNP製剤にはアジュバント効果もあります
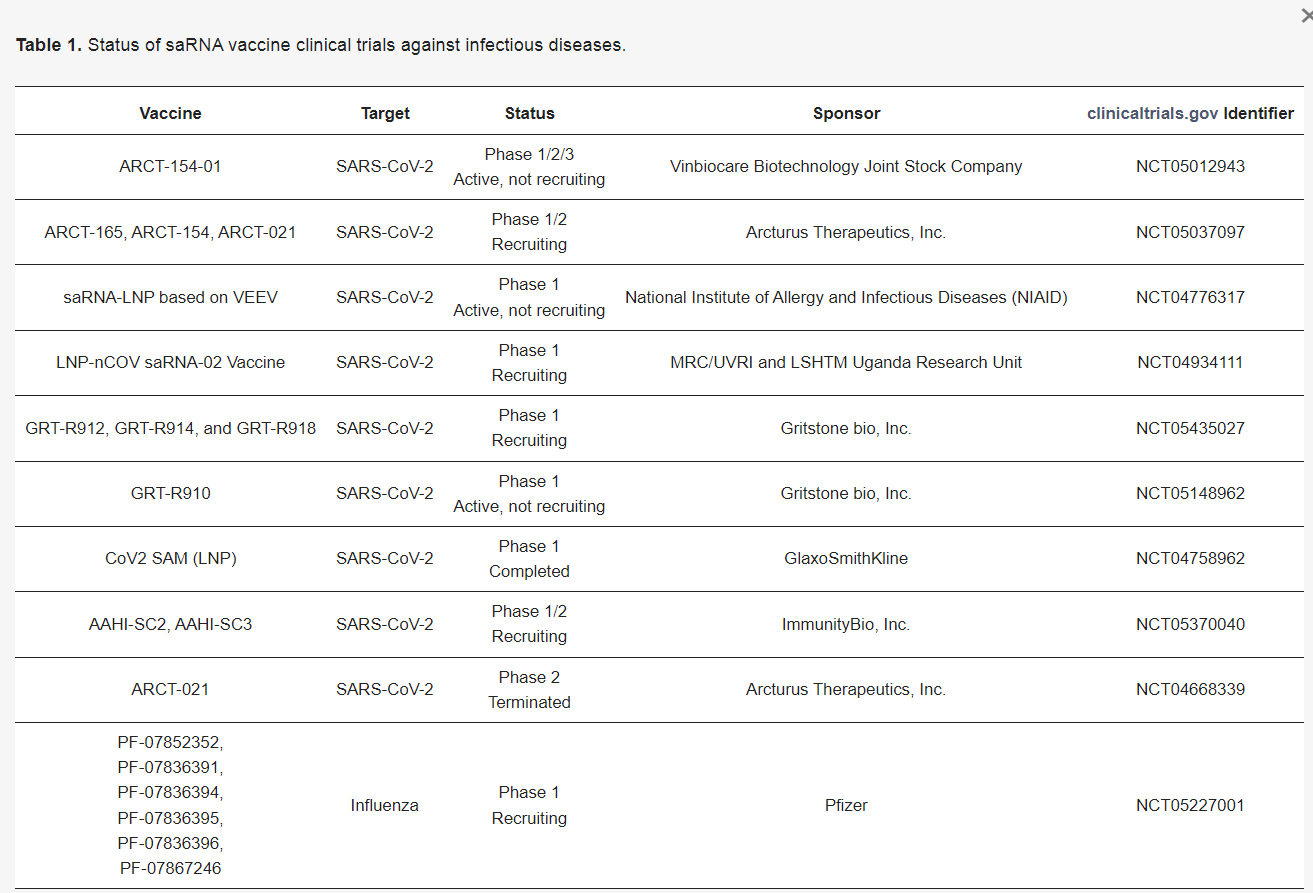
sa-mRNA をパイプラインに持つ企業:
私の懸念…自己増幅 mRNA の脱落
- ファイザーは、自社製品が脱落し、吸入または皮膚接触による「環境暴露」を引き起こすことを認めた。

- しかし、LNP/mRNA またはエキソソーム/mRNA を介して少量のファイザーまたはモデルナの新型コロナウイルス感染症 (Moderna) mRNA ワクチンに曝露された場合、ワクチンは接種されません。
- 免疫システムがそれを破壊します。
- しかし、自己増幅型 mRNA の放出にさらされたらどうなるでしょうか?
- 理論的には、その mRNA は 1 か月間、体内で未知の量の自身のコピーを作成する可能性があり、それは永続的な内部損傷を引き起こすのに十分な長さである可能性があります。
- このリスクは研究されていません。

まとめ
日本は世界初の新型コロナウイルス感染症(COVID-19)自己増幅型sa-mRNA新型コロナウイルスワクチンを承認した。
このテクノロジーには次のような問題があります。
- mRNA の用量は少ないですが、スパイクタンパク質の量は多く、副作用プロファイルはファイザー mRNA と同じです。利益?大手製薬会社の生産コストの削減。
- Arcturus はファイザーと同様に独自の脂質ナノ粒子 (LNP) を使用していますが、生体内分布や安全性に関する研究は行われていません。
- これらの LNP は、血液脳関門や胎盤関門を越えて、外来のシュードウリジン修飾 sa-mRNA を全身に送達します。
- あなたの体を単なるスパイクタンパク質の工場ではなく、スパイクsa-mRNAとスパイクタンパク質の生産工場に変えます。
- DNA プラスミドの汚染も依然として発生します
- sa-mRNA はファイザー mRNA の 3 倍の長さ(独自の複製機構のための追加のコードのため)、これは製造中に不純物のリスクが高いことを意味します
- 精製がさらに困難になるため、DNA汚染はさらに深刻になる可能性があります
- ベネズエラ馬脳炎ウイルス(VEEV)のゲノムを複製機構に使用する
- 欠陥のあるsa-mRNA配列が体内で増幅され、未知の結果をもたらす変異タンパク質が生成されるリスクが増加します。
- sa-mRNA は細胞内で最長 1 か月間、未知の量まで増幅されます (元の sa-mRNA はプソイドウリジン修飾されていますが、細胞内で作られたコピーは修飾されていないためです)
- sa-mRNA 増幅の忠実度は不明であり、テストされていません
- 未知の量のスパイクタンパク質を生成します
- 未知の量の変異したスパイクタンパク質と未知の非スパイクタンパク質を生成します。
- 小田氏による日本の研究では、ファイザー製の新型コロナウイルス感染症追加免疫療法と同じ副作用プロファイルが示されている(これは悪い兆候だ)
- 彼らはRNAワクチン候補を迅速に生産することができ、インフルエンザワクチン候補はわずか8日で生産されたと報告されました(これも悪い兆候です)
- 研究では、mRNAが宿主ゲノムに組み込まれるリスクはないと主張されていますが、それを裏付ける証拠はありません
- 免疫応答を刺激するdsRNA中間体を生成しますが、その効果(および副作用)は完全には理解されていません。
- 自己増幅型 mRNA では、脱落はさらに危険になります。
- 脱落した人は、約 1 か月間、未知の量の sa-mRNA を生成し始め、永久的な損傷を引き起こす可能性があります。
- 最後に、sa-mRNA 全体がゲノムに組み込まれると、スパイク mRNA が無限に増幅される (そしてスパイクタンパク質が生成される) ことになります。
- 長期的な安全性研究は行われていません。
この自己増幅 mRNA 技術は、ファイザーとモデルナの新型コロナウイルス感染症 mRNA ワクチンで経験したことよりもさらに大きな災害のように思えます。
興味がありません。