「patisiran」は2018年8月10日、世界で初めて「成人の遺伝性トランスサイレチン型(hATTR)アミロイドーシスによる多発性神経障害(=ポリニューロパチー)」治療薬として、米食品医薬品局(FDA)から「ONPATTRO」の商品名で承認を取得している。
日本国内では、希少疾病用医薬品に指定されており、Alnylam Japan株式会社は2019年半ば頃の承認取得を目指している。

遺伝性トランスサイレチン型アミロイドーシスポリニューロパチー治療薬
(トランスサイレチン型家族性アミロイドーシス)
RNAi(RNA interference=干渉)治療薬「patisiran(パティシラン)米国名:ONPATTRO」
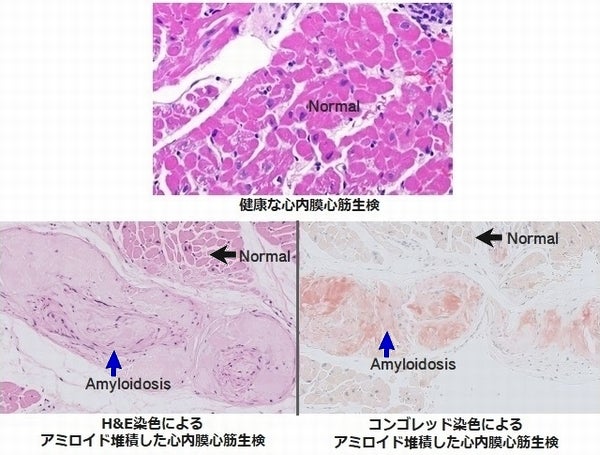
遺伝性(hereditary)トランスサイレチン型アミロイドーシスポリニューロパチー(hATTR-AP)は、トランスサイレチン(TTR)遺伝子(第18染色体)の突然変異が原因となり、末梢神経と自律神経に高度のアミロイド(線維状蛋白)沈着が起こり、進行期には、心臓、消化管、腎臓、眼など、全身の組織への異常なアミロイドタンパク質が蓄積し、機能障害を起こす疾患です。
診断からの生存期間中央値は4.7年。発症から平均10年で死亡に至る予後不良な疾患です。
トランスサイレチン(TTR)遺伝子変異はこれまで100種類以上報告されていますが、国内では約80パーセントがV30M型であり、長野県と熊本県に集積地が存在している。〔日本神経学会--遺伝性ATTRアミロイドーシスの治療の現状と今後の展望より/公益財団法人 難病医学研究財団/難病情報センター・指定難病28/全身性アミロイドーシスより〕
長野県と熊本県の集積地では、20~40歳での発症が多いようですが、散発的に発生する孤発家系の患者は、全国各地から多数報告されています。
遺伝性トランスサイレチン型アミロイドーシスは、常染色体優性遺伝を示し、世界中で約5万人が罹患しており、日本国内では、未診断の患者も含めると患者数は700名と推定されています。〔ファイザー株式会社:TTR-FAPの定義・病態・疫学より〕
尚、遺伝性トランスサイレチン型アミロイドーシスポリニューロパチーは従来、家族性アミロイドポリニューロパチー(Familial Amyloid Polyneuropathy; FAP)と呼ばれていましたが、国際アミロイドーシス学会(International Society of Amyloidosis Symposium)は、hereditary-ATTR amyloidosisの病名を用いる事を推奨しており、家族型の表記が改定されており、本記事でもこれに従っています。
疾患の原因となるTTR(トランスサイレチン)タンパク質は、主に肝臓で産生される血漿タンパクで、通常はビタミンA(レチノール)の輸送に関与している。
TTR遺伝子の突然変異は、異常なアミロイドタンパク質を蓄積させ、難治性の末梢感覚運動神経障害、自律神経障害、または心筋症などの他の疾患が発現する。
心臓では心筋症の発症や房室ブロックによって、ペースメーカーの埋込みが必要となる。
治療法としては、[①]遺伝子変異のあるTTRの95%以上は肝臓で作られているため、発症早期に肝臓移植を行う事が、病気の進行を抑える有効な治療法です。
薬物療法では、[②]遺伝性トランスサイレチン型アミロイドーシスの疾患の経過を変更する事が出来る薬剤として唯一の承認薬:ビンダケル®カプセル20mg(ファイザー=末梢神経障害の進行抑制/1カプセル=5万7171円)がありますが、病気の原因であるアミロイドの沈着を抑える事は出来ません。
その他の病状については、[③]臓器ごとの対症療法に限られており、治療を良好に助けるための、新機序医薬品の登場が切実に望まれています。
今回承認申請した「patisiran(パティシラン)/ONPATTRO™」は、2006年ノーベル生理学・医学賞を授賞した『RNA干渉(interference)の発見(発見されたのは1998年)』に基づいて、トランスサイレチン(TTR)を標的とするRNAi治療薬です。
▲RNA干渉とは‥‥、標的遺伝子と同じ配列をもつ2本鎖のRNA(リボ核酸)を細胞内に導入すると、mRNA(メッセンジャーRNA)が分解され、遺伝子の発現が抑制される現象です。標的となるmRNAを分解させる事が出来るため、癌やエイズ、遺伝病の治療などへの応用が期待されている。
「patisiran(パティシラン)」は、特定のmRNA(メッセンジャーRNA)を標的とし、肝臓に於けるトランスサイレチン(TTR)の産生をブロックするように設計されており、TTRタンパク質が産生される前に産生を阻害し、病気の進行を止めたり遅くする事で、体内組織や臓器へのTTRタンパク質の蓄積を減少させるとしている。
「patisiran(ONPATTRO™)」の重要安全情報。
■輸液関連反応(IRR=薬剤投与中または投与後24時間以内に多く現れる有害事象の総称)
「patisiran」で治療された患者には、輸液関連反応(IRR)が観察されている。
制御された臨床試験では、本剤の治療患者の19%がIRRを経験した。本剤のIRRの最も一般的な症状は、潮紅、背中の痛み、吐き気、腹痛、呼吸困難、及び頭痛であった。
IRRのリスクを減らす為に、患者は本剤注入の少なくとも60分前に、副腎皮質ステロイドホルモン、パラセタモール(アセトアミノフェン)、及び抗ヒスタミン剤(H1/H2ブロッカー)で前投薬を受ける事を勧める。
輸液中の患者をIRRの徴候および症状についてモニターする。
IRRが発生した場合は、臨床的に指示されているように、輸液の減速または中断と医療管理の導入を検討すること。
輸液が中断された場合は、症状が改善した場合にのみ、注入速度を遅くして再開することを検討する。 重篤な、又は生命を脅かすIRRの場合、輸液は中止し、再開をしない。
▲これらの有害事象(副作用)は米食品医薬品局(FDA)で承認された際の注意安全情報の直訳であり、日本国内では未承認なため、用法・用量などは明らかではありません。
あくまで参考程度にとどめて下さい。