傍腫瘍症候群に関してMayo Clin Proc. 2010 Sep; 85(9): 838–854を読みました。
内容が膨大ですので何回に分けて掲載します。
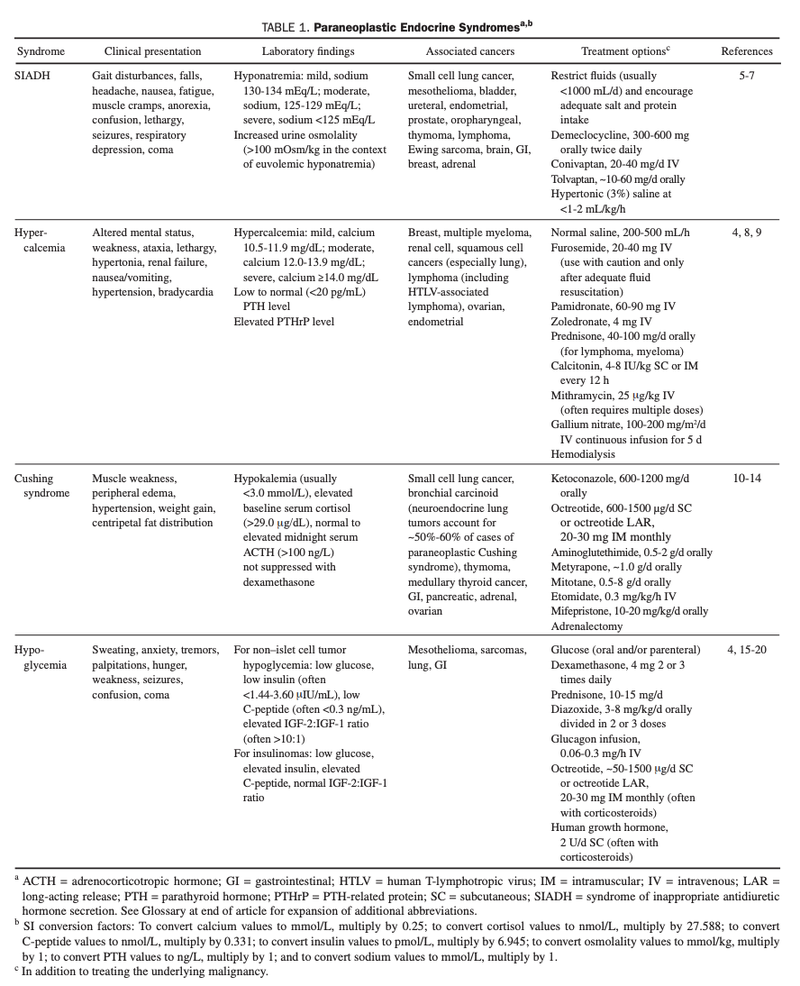
このレビューでは内分泌・神経・皮膚・リウマチ・血液に分けて記載されていました。今回は内分泌に限定して掲載です。
高Ca血症に関してはNEJMに悪性腫瘍の高Ca血症のレビューに詳細な機序の掲載がありますのでおすすめです。(N Engl J Med. 2022 Apr 14;386(15):1443-1451.)
〜内分泌症状〜
腫瘍によるホルモン・ペプチド産生に起因し腫瘍の治療による改善されることが多い
ーSIADHー
抗利尿ホルモン不適合分泌症候群 (SIADH) は、低浸透圧の正常循環性低ナトリウ ム血症を特徴とし、すべてのがん患者の 1% から 2% に影響を与える。
小細胞肺癌がこれらの症例のほとんどを占めており、小細胞肺癌の全患者の約 10% から 45% が SIADH を発症する。
癌患者では消化管からの損失、過剰な利尿、副腎機能不全、塩分喪失性腎症、CSWも癌患者では起こる可能性があるが全て体液量減少性の低Na血症となる。
根底の腫瘍を治療すると数週間でNaは正常化する。頻度の多い薬剤(アヘン・抗うつ薬・ビンアルカロイド・シスプラチン)の中止が必要となることもある。
ー高Ca血症ー
悪性腫瘍関連の高カルシウム血症は、進行がんの全患者の最大 10% に発生し、一般的に予後不良である。高カルシウム血症のがん患者の 30 日死亡率は約 50%である。
癌患者における高カルシウム血症の主な機序は 4 つである。悪性腫瘍の体液性高カルシウム血症として知られる腫瘍細胞による副甲状腺ホルモン (PTH) 関連タンパク質 (PTHrP) の分泌は、症例の 80% を占め、扁平上皮腫瘍で最も一般的に発生する。骨と腎臓の PTH 受容体に結合すると、PTHrP は骨吸収とカルシウムとリン酸の腎臓処理する。
別の20%の症例は、骨格転移部位での溶骨性変化から直接発生する。乳がん、多発性骨髄腫、リンパ腫は、一般的にこのメカニズムを介して高カルシウム血症を引き起こす。
まれに、特定のリンパ腫に関連して報告されているビタミン D の腫瘍分泌、または PTH の異所性腫瘍分泌から高カルシウム血症が生じる
高カルシウム血症の臨床的特徴には、吐き気、嘔吐、無気力、腎不全、および昏睡が含まれる。
高カルシウム血症のすべての患者が積極的な治療を必要とするわけではないため、治療の必要性と治療の性質は、これらすべての要因を考慮に入れる必要がある。
悪性腫瘍に関連した高カルシウム血症の患者では、典型的な検査所見には、カルシウム濃度の上昇、PTH 濃度が低から正常、そしてしばしば PTHrP 濃度が高い。
治療
可能であれば、高カルシウム血症の原因となる薬物療法(例、カルシウムサプリメント、ビタミンD、サイアザイド系利尿薬、カルシウム含有制酸薬、およびリチウム)または精神状態の変化を悪化させる薬物療法を中止。
持続性高カルシウム血症に対する第一選択のアプローチは、通常の生理食塩水による体液補充である。十分な脱水の補正をしてから利尿薬は使用する。
パミドロネートやゾレドロネートなどのビスフォスフォネートの静脈内投与は、破骨細胞の骨吸収を阻害し、有効性と毒性プロファイルが良好であるため広く使用されている。
ークッシング症候群ー
クッシング症候群 (コルチゾール亢進症) の症例の約 5% から 10% が腫瘍随伴性の可能性がある。これらの随伴性症例の約 50% から 60% は、神経内分泌肺腫瘍 (小細胞肺癌および気管支カルチノイド) である。
SIADH や高カルシウム血症とは対照的に、がんの診断が下される前に、腫瘍随伴性クッシング症候群の症状が現れることがある。
腫瘍随伴性クッシング症候群は、副腎皮質刺激ホルモン、コルチコトロピン放出因子の腫瘍分泌から生じる。これらの要因により副腎からコルチゾールが産生、放出される。
高血圧、低カリウム血症、筋力低下、および全身性浮腫を特徴とする。
関連する検査所見としては、ベースラインの血清コルチゾール値が29μg/dL以上、尿中遊離コルチゾール値が47μg/24時間以上、深夜副腎皮質刺激ホルモン値が100ng/L以上である。
高用量のデキサメタゾン抑制に反応しない場合は、異所性(腫瘍随伴性)クッシング症候群と下垂体からのクッシング症候群を区別する。
ーhttps://www.jmedj.co.jp/premium/treatment/2017/d100401/よりー
根底にある腫瘍の治療とは別に、腫瘍随伴性クッシング症候群の第一選択の薬理学的オプションは、ステロイド産生の阻害である。
これらの薬には、ケトコナゾール、ミトタン、メチラポン、およびアミノグルテチミドが含まれる。降圧剤と利尿剤は、血清カリウムを注意深く監視しながら、症状をコントロールするために使用することがある。
一般的ではないがオクトレオチドとエトミデートが使用されることがある。薬物療法がうまくいかない場合は、副腎摘出術が考慮されることがある。
ー低血糖症ー
腫瘍関連低血糖はめったに発生せず、インスリン産生膵島細胞腫瘍および (傍腫瘍性) 膵外腫瘍によって引き起こされる可能性がある。
後者は非島細胞腫瘍性低血糖症(NICTH) と呼ばれ、20 mg/dL (mmol/L に換算すると 0.0555 を掛ける) という低血糖レベルの再発性または持続性の低血糖エピソードとして現れ、典型的には高齢患者に起こる。
これらの低血糖エピソードは、根底にある腫瘍の診断よりも前に発生する可能性がある。
非膵島細胞腫瘍の低血糖は通常、IGF-2 の腫瘍細胞産生によって引き起こされますが、インスリンの腫瘍細胞産生によっても発生する。
NICTH の低血糖はIGF2の腫瘍産生細胞によって引き起こされ、低血清インスリンレベル ・Cペプチド・低レベルの成長ホルモン・IGF-1、IGF-2の上昇が見られる。
NICTH に対する最適な初期アプローチは、根底にある腫瘍を治療する (可能であれば切除する)のようなアプローチが実行できない場合、医学療法の目標は適切な血糖値を維持する
切除が不可能であれば適切な血糖値を維持する。
再発性または慢性の低血糖エピソードの長期管理には、コルチコステロイド、成長ホルモン、ジアゾキシド、オクトレオチド、グルカゴンが使用される。
長くて読みづらくて申し訳ありません。比較的まとまったいいレビューかと思います。